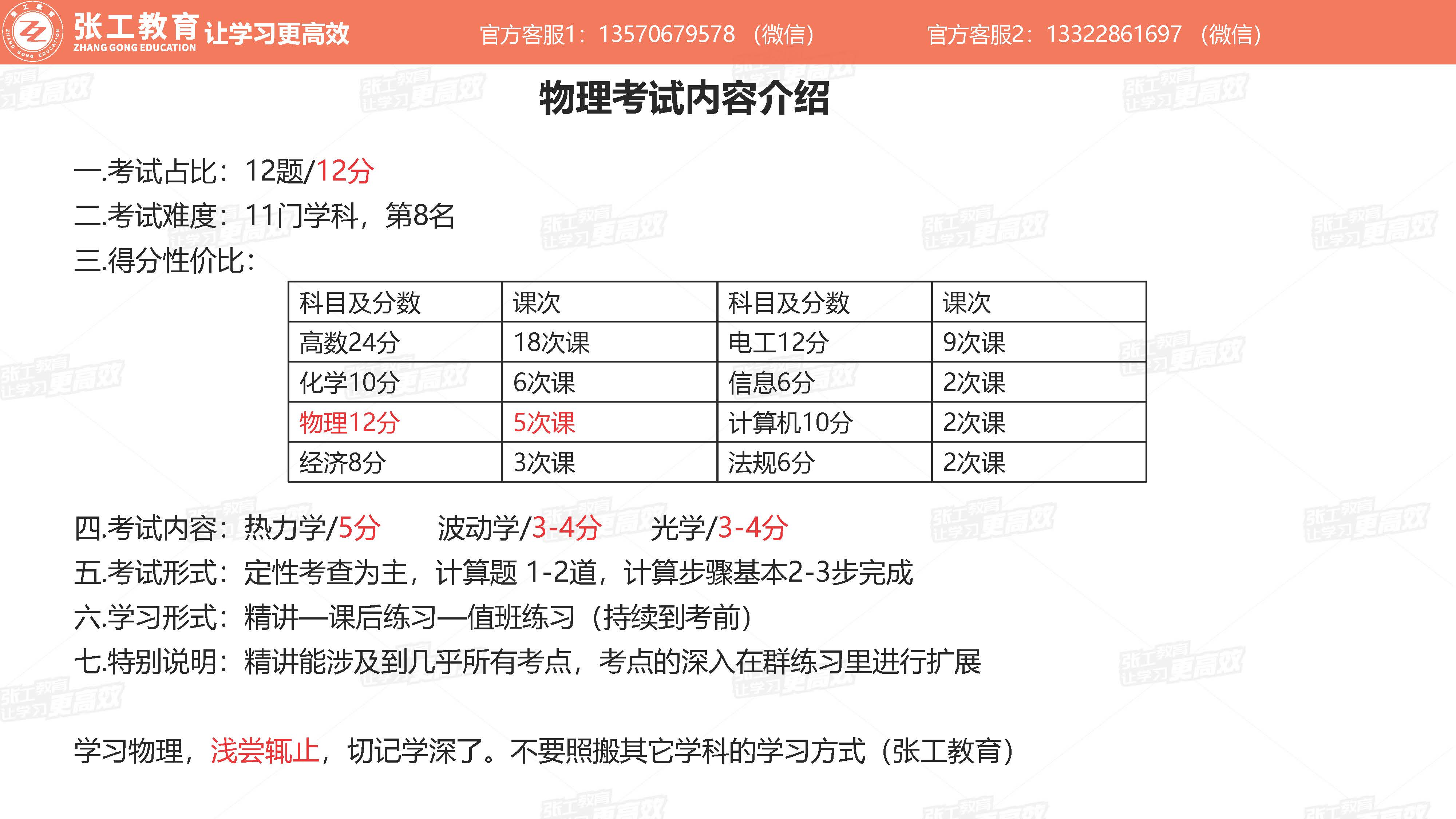
普通物理(12分)
考试快速做题指南
- 定型考察为主,计算题1-2道,计算步骤基本2-3步完成
- 出的所有题目在百度上都能找到(专家自己不出题)
- 学习物理,浅尝辄止,切记学深了(只做课后题,不要做其他题目了)
热力学1(5分)
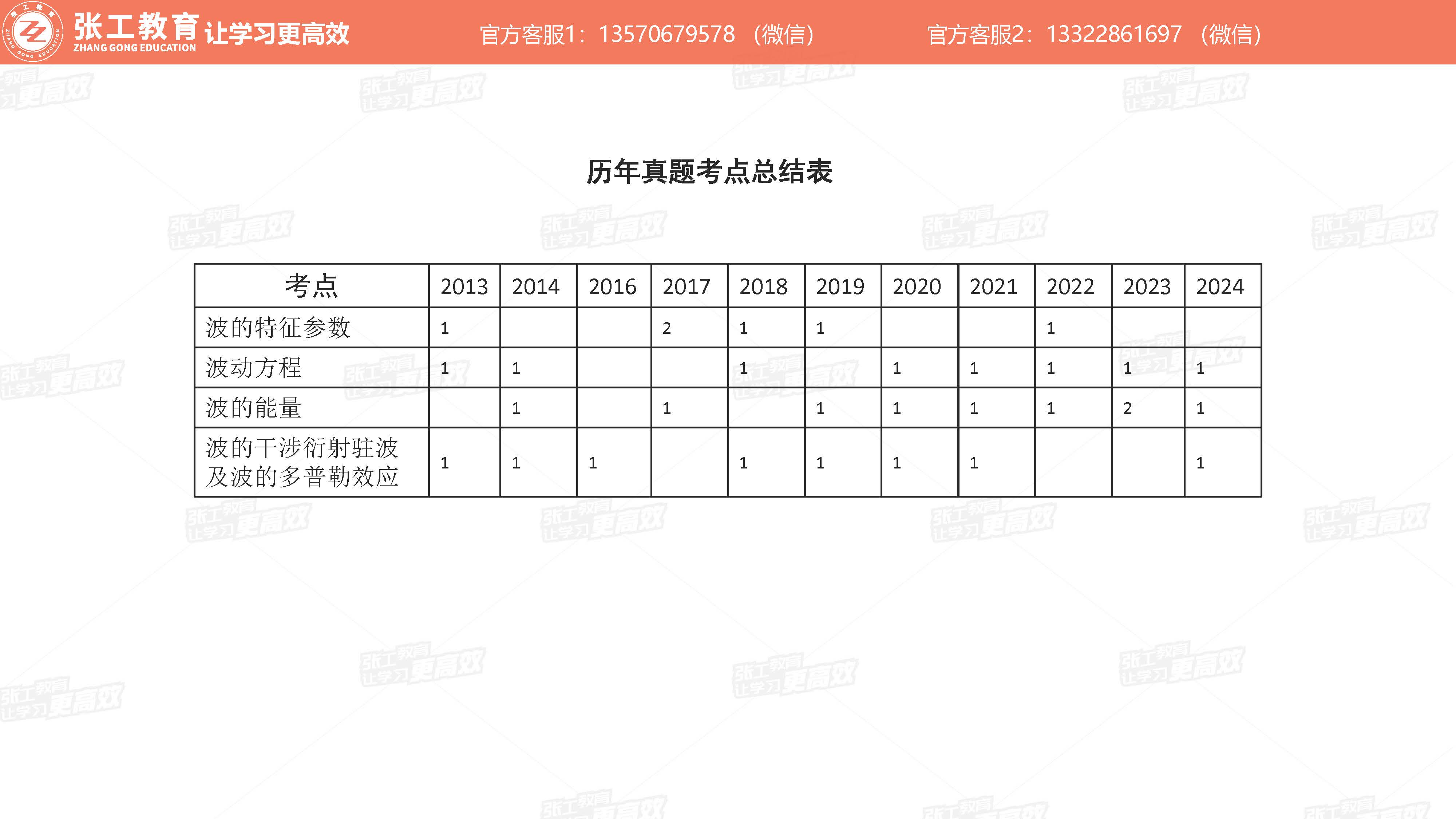
历年真题考点总结表
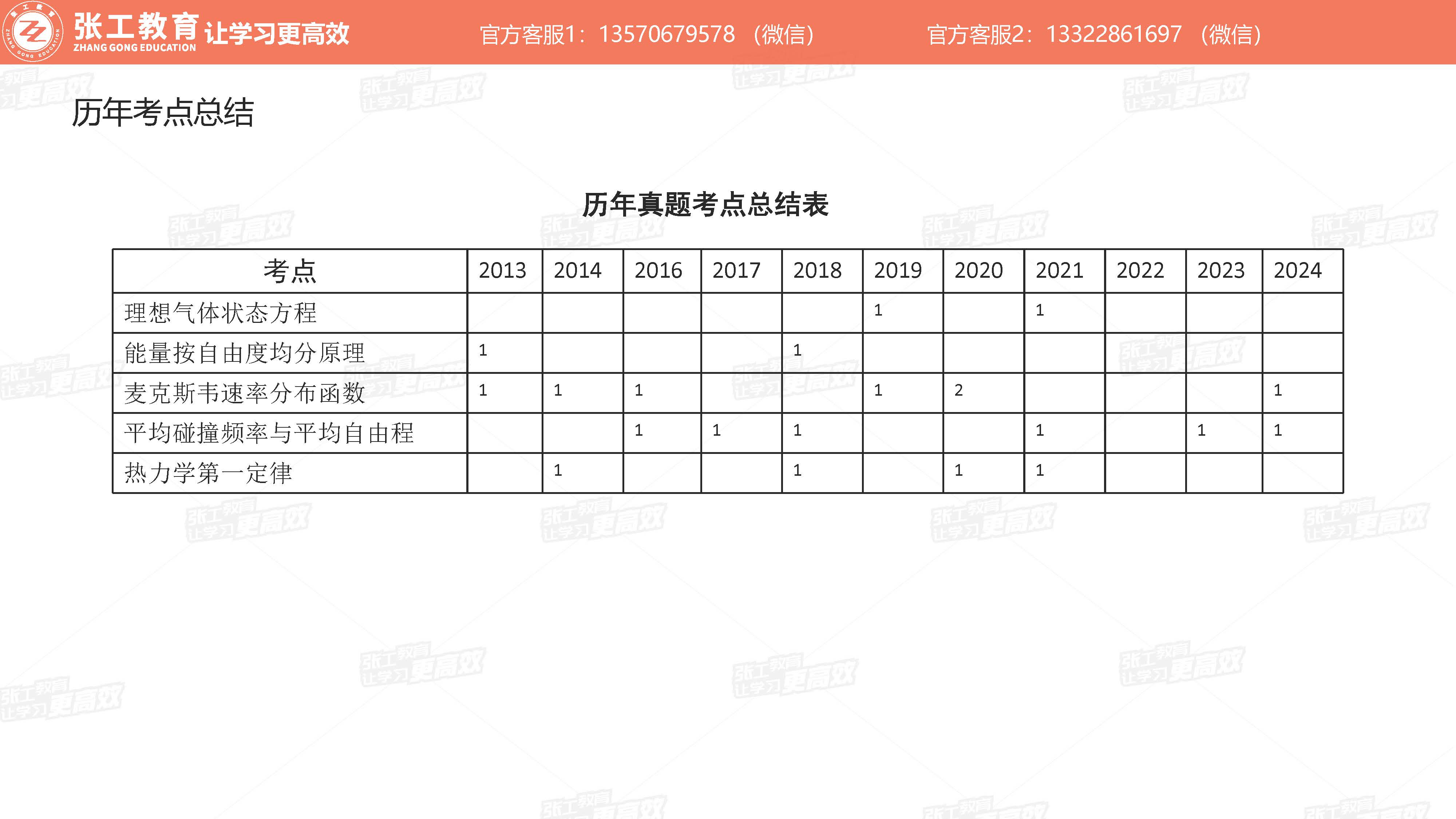
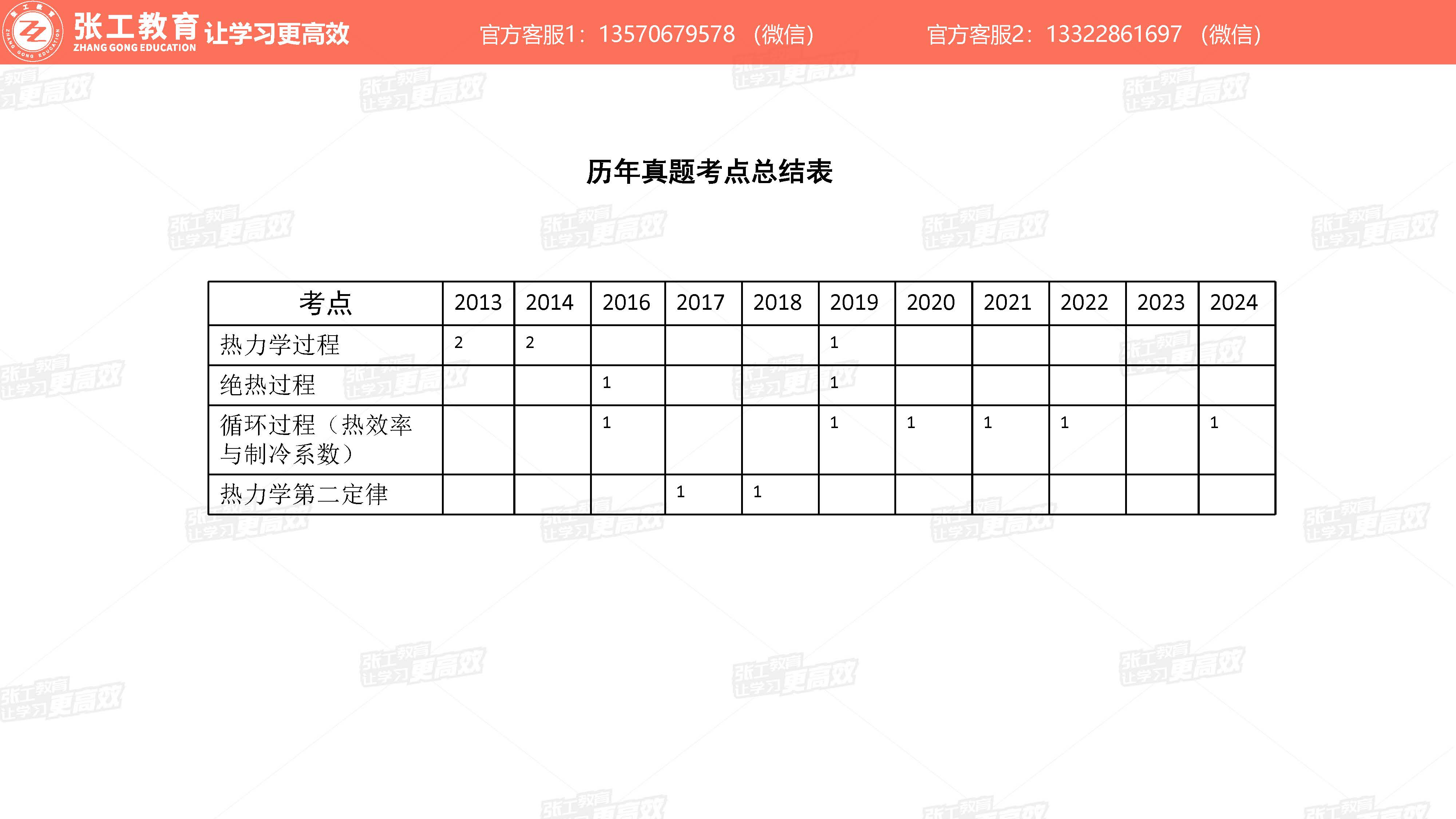
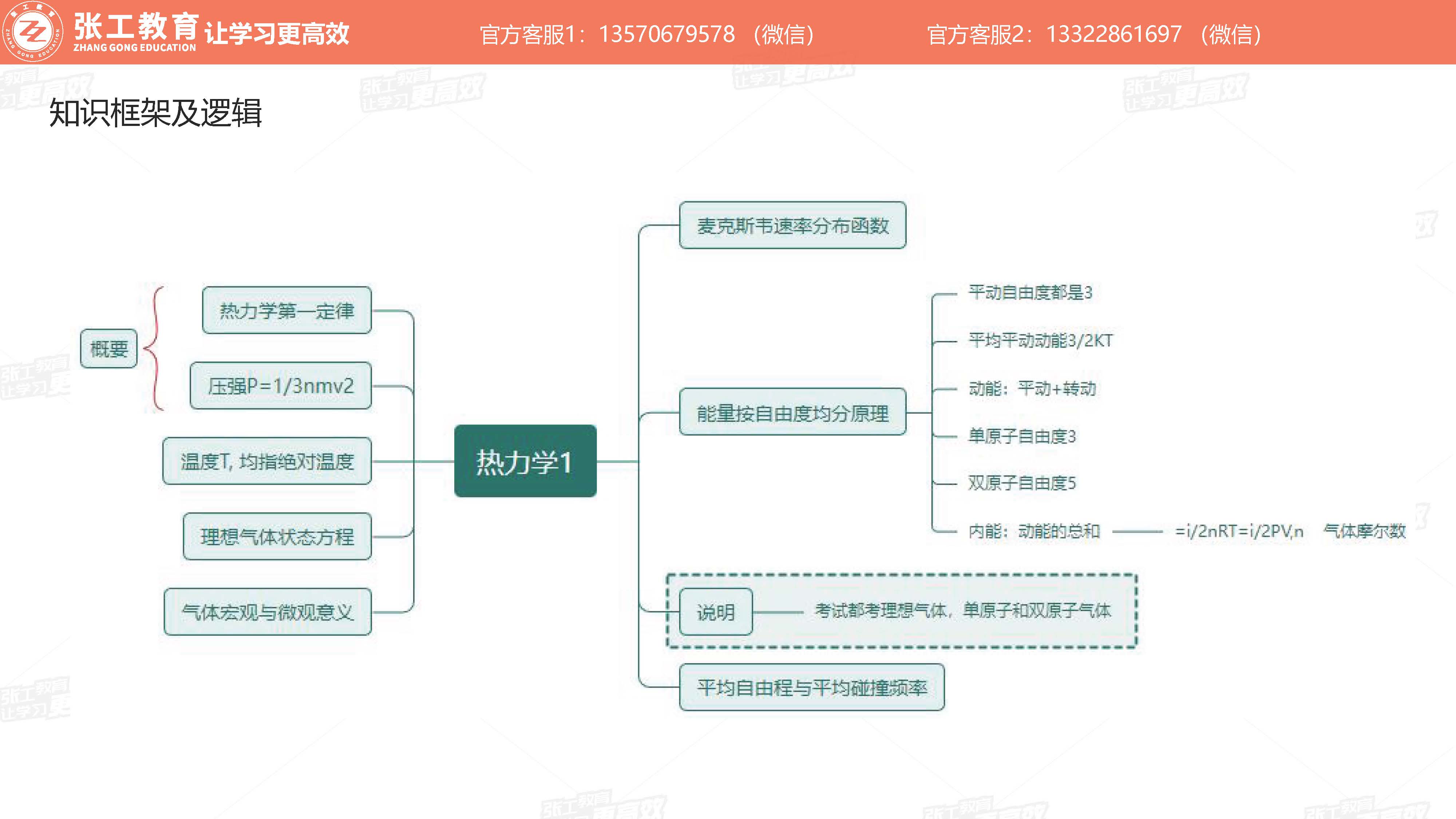
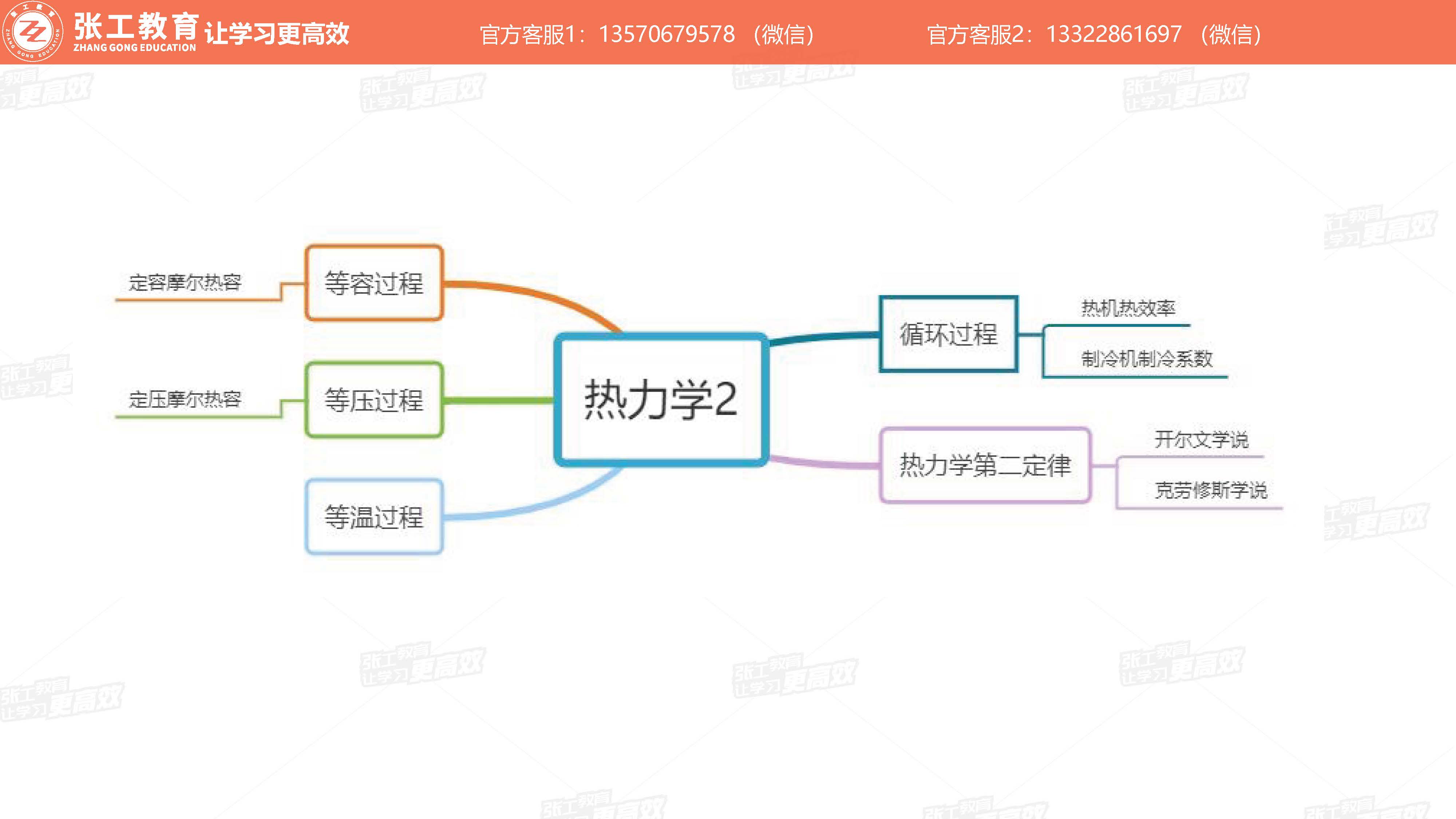
物理课程相关名词
- 摩尔
- 摩尔质量
- 分子数密度n
- 气体的原子量或摩尔质量
- 氢气
:分子量2 - 氦
:原子量4 - 氮
:分子量28 - 氧
:分子量32 - 二氧化碳
:分子量44
- 氢气
- 热力学温度(开尔文)
- 各种符号对应的字母
- 气体:
- 波动学与光学:
- 气体:

基本概念
- 考点1:热力学系统
- 考点2:平衡态4个特点
- 考点3:状态参量(P,T,V不会进行定量计算)
- 温度T(热学描述)
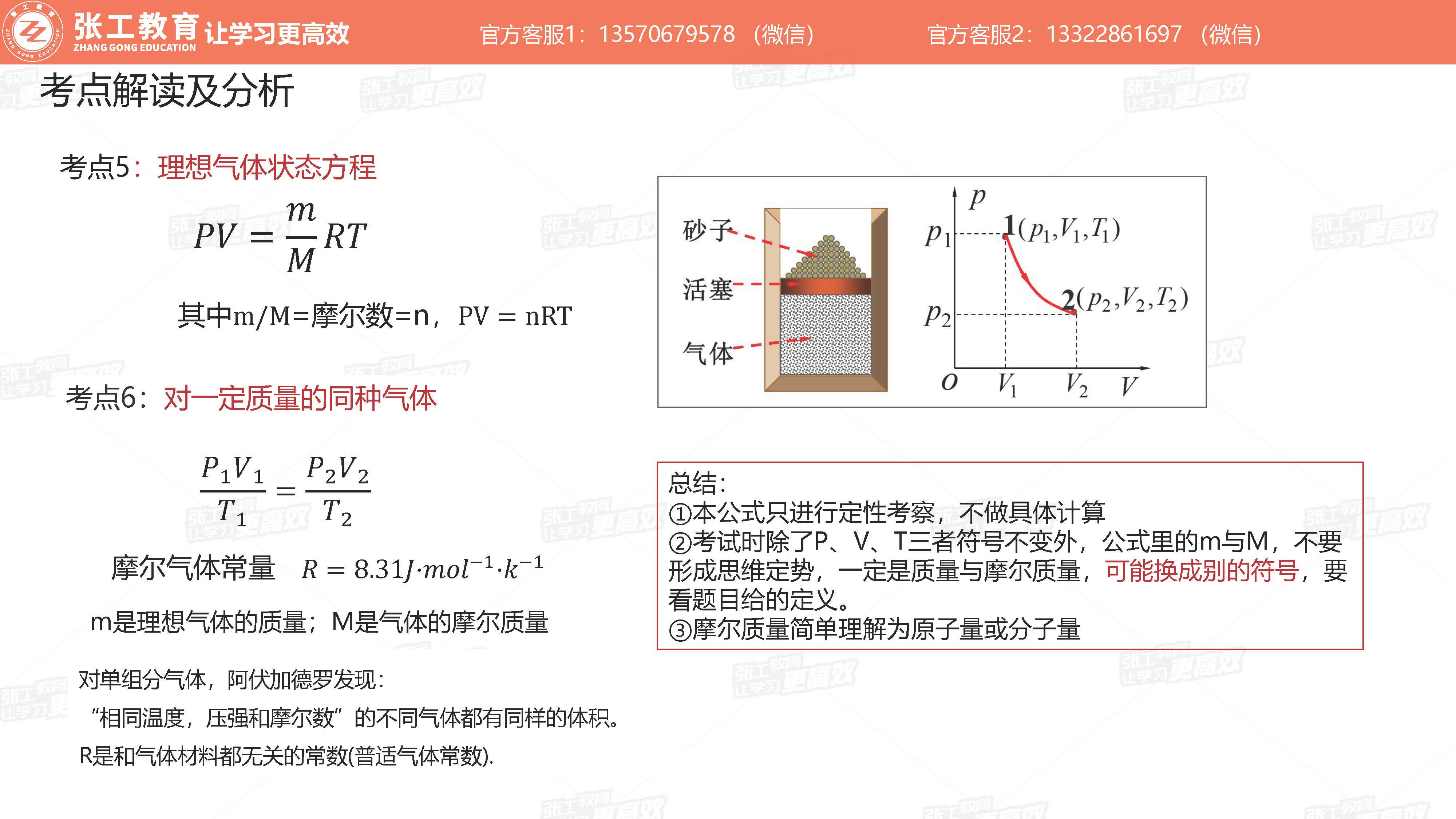
- 体积V(几何描述):标准状况的参数、容器的体积
- 热力学过程(包含许多中间状态)
- 平衡过程(准静态过程)
- 压强P(力学描述):气体分子对器壁碰撞的统计平均表现。
- 平衡过程
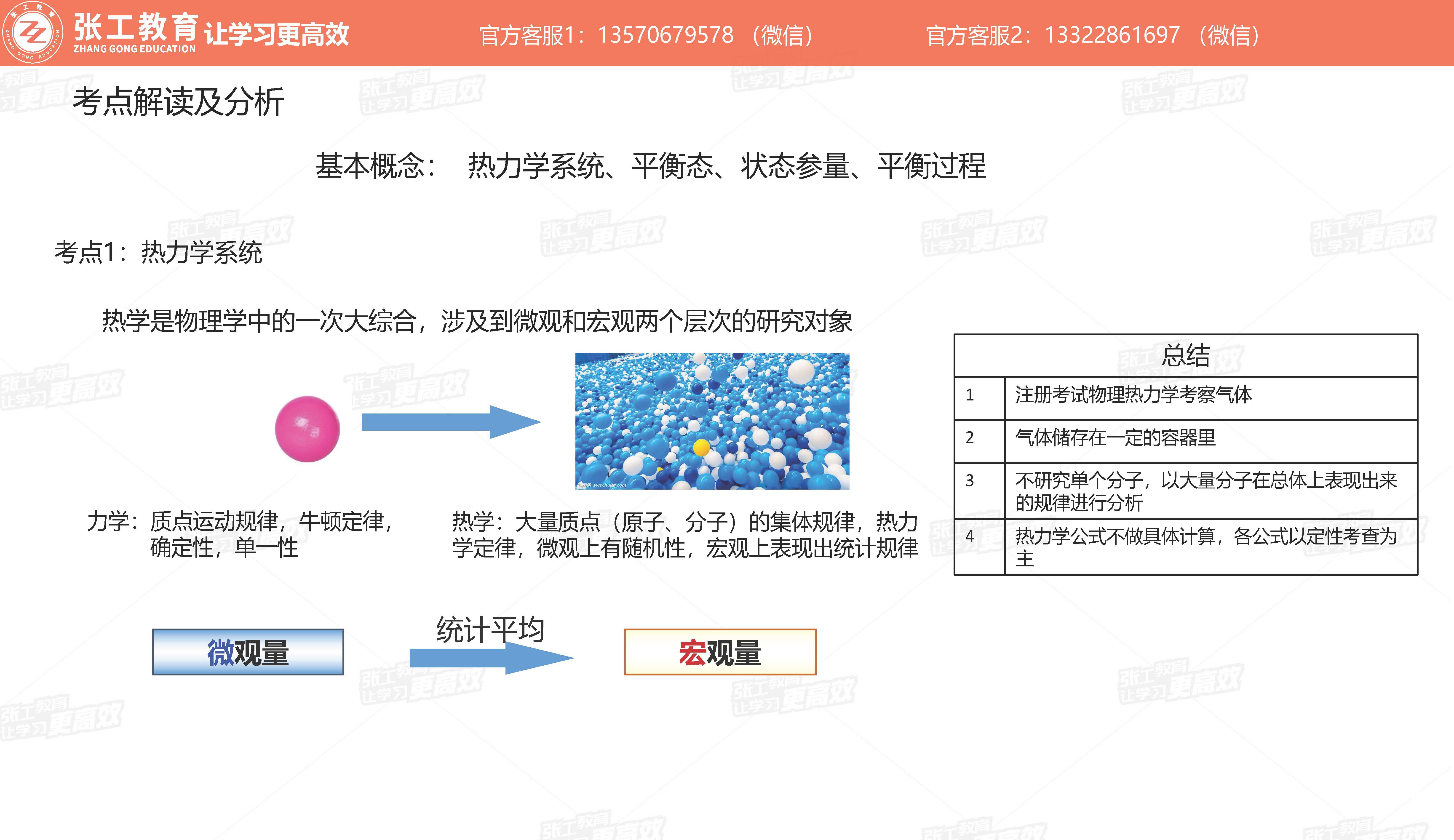

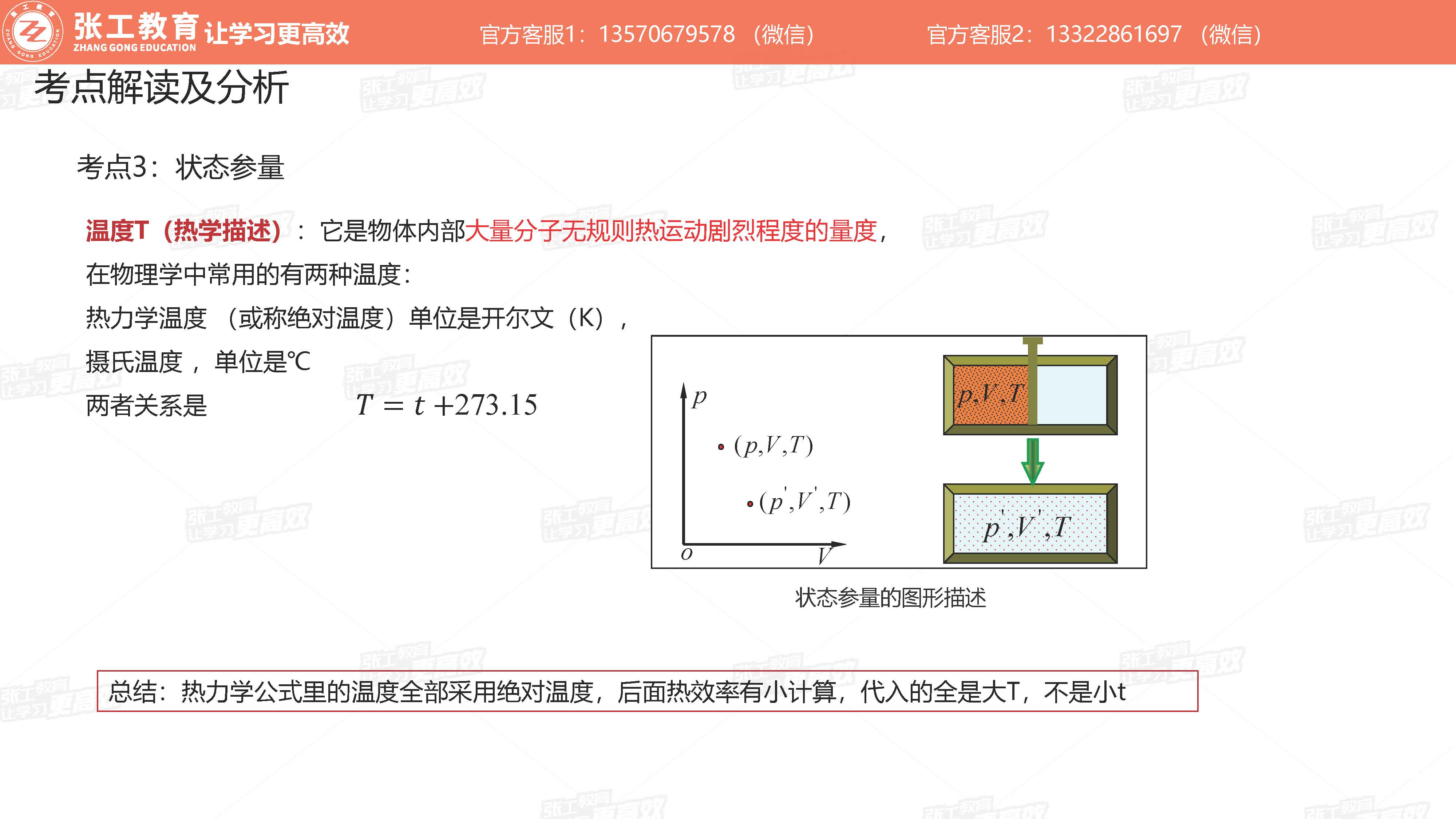

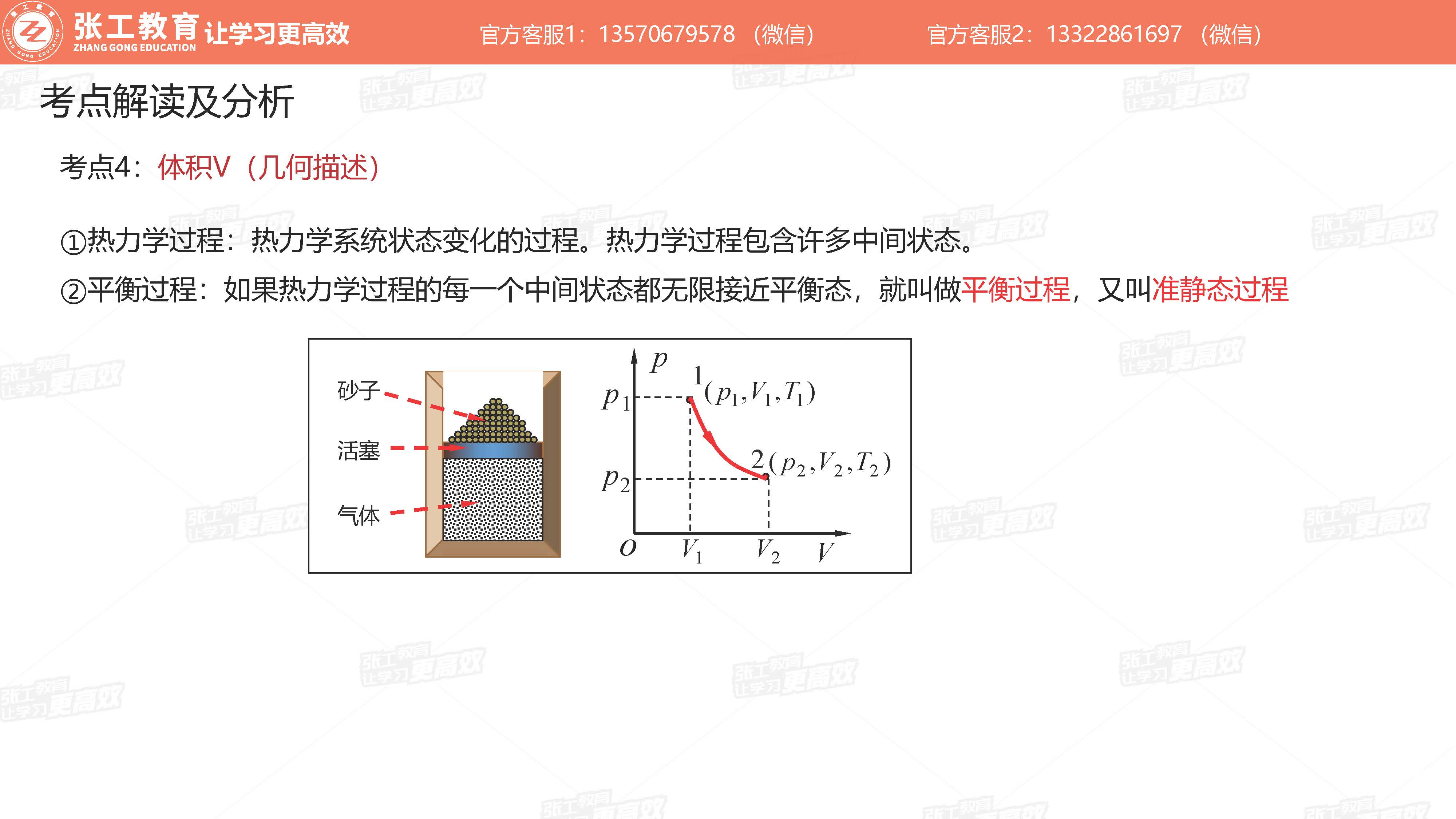
理想气体状态方程
理想气体 理想气体是考试出题的常用字眼,是热力学公式应用的前提条件,对理想气体本事的性质不进行考察。
压强的定义(可能的考点) 理想气体与器壁碰撞过程中气体分子在单位时间里施加于器壁单位面积冲量的统计平均值,宏观上表现为气体的压强。
理想气体状态方程 本公式只进行定型考察,不做具体计算。 考试时除了P、V、T三者符号不变外,公式里的m与M不要形成思维定势,一定是质量与摩尔质量,可能换成别的符号,要看题目给的定义。
玻尔兹曼常数:
阿伏伽德罗常数(1mol气体分子数):
普适气体常数(和气体材料无关):
能量按自由度均分原理
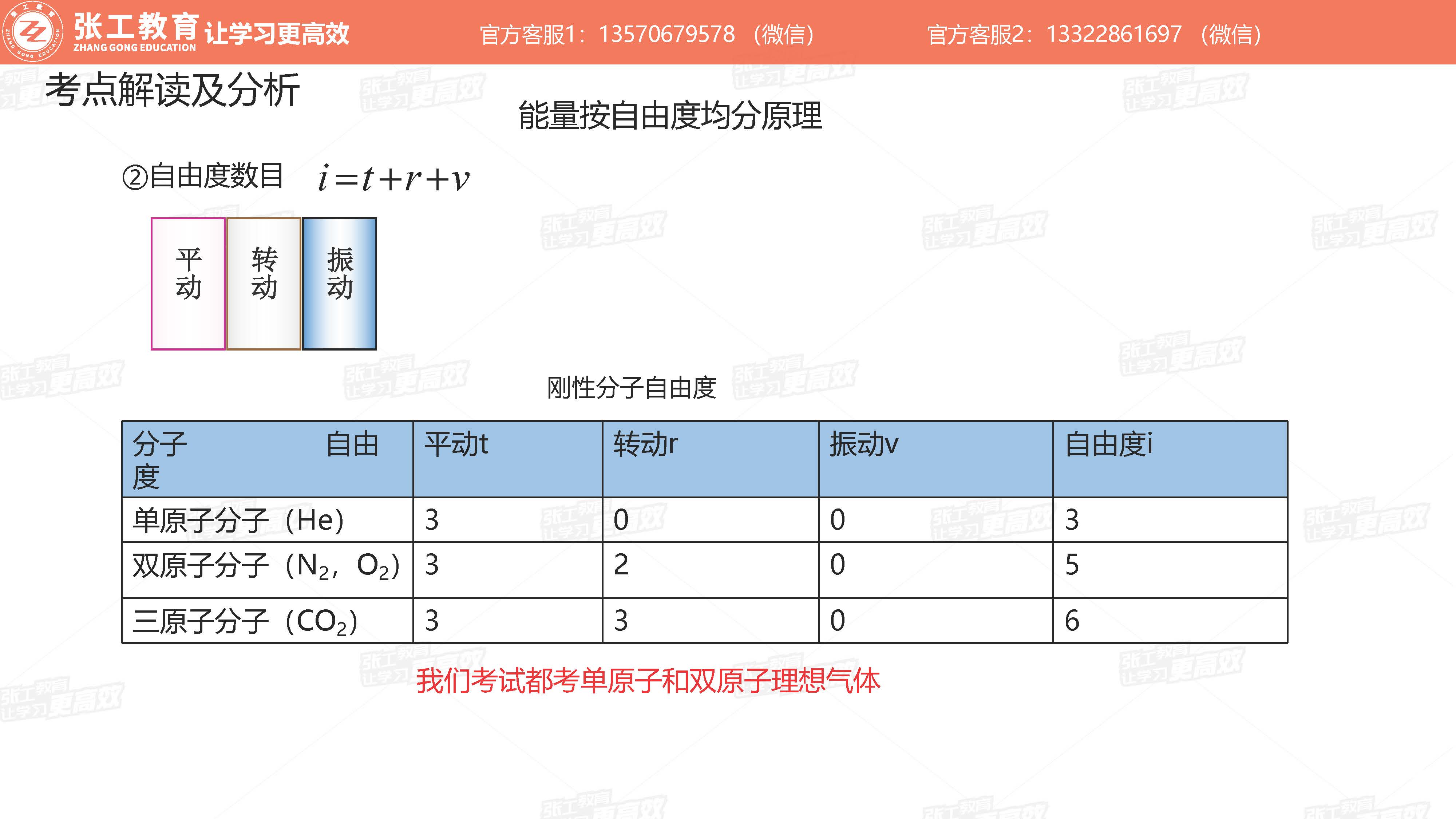
- 自由度数目
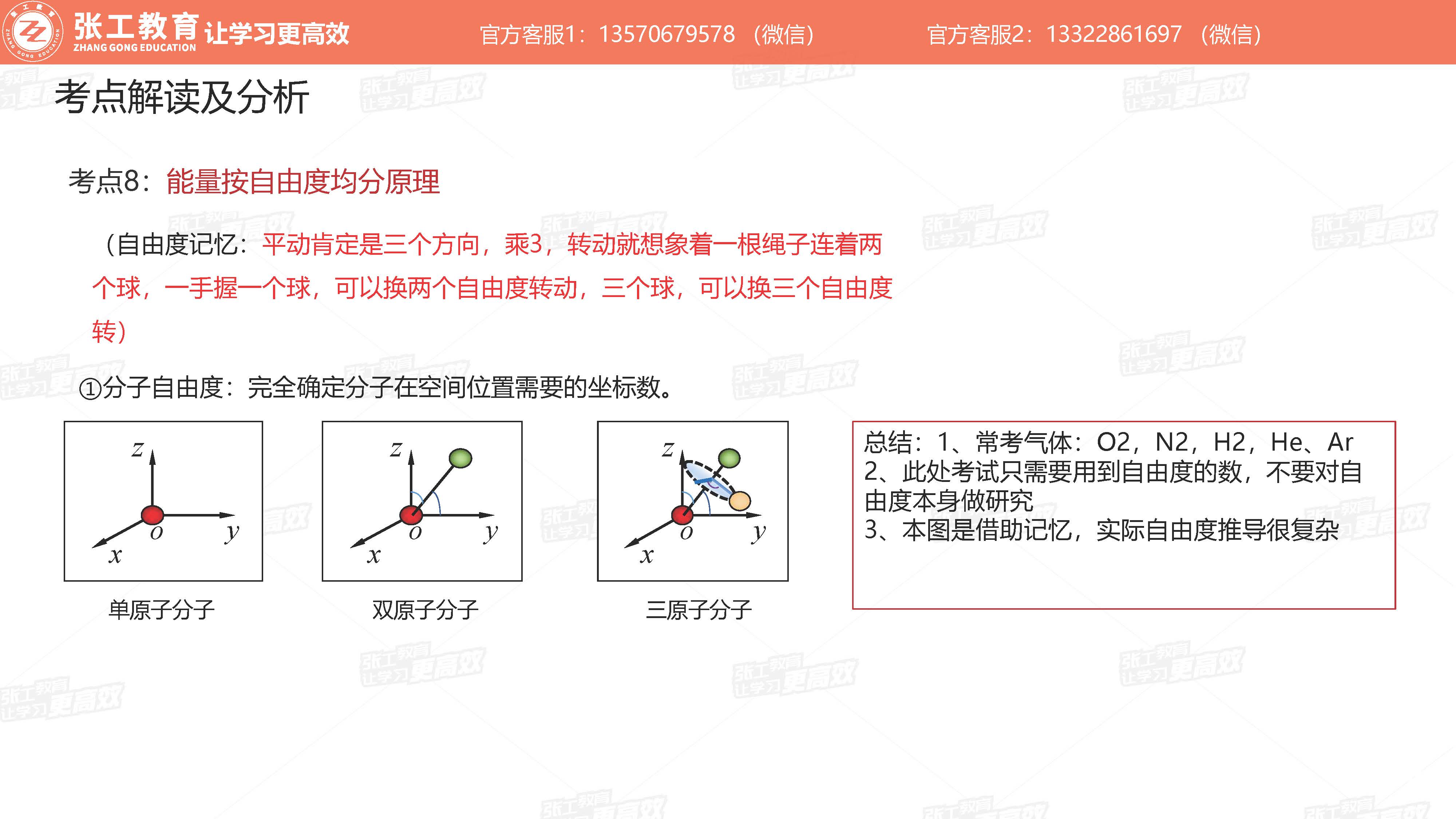
- 分子自由度(平动3个+转动+振动(本考试不考虑))
- 单原子(3个)
- 双原子(5个)
- 三原子分子(6个)
- 平动自由度:3个
- 平均动能、平均平动动能、内能
- 分子动能、平动动能
- 分子的每一个自由度都具有相同的平均功能,其大小都等于
- 分子的平均功能
- 分子的每一个自由度都具有相同的平均功能,其大小都等于
- 考点9:理想气体的压强和温度
- 温度是气体分子平均平动动能的量度
- 分子的平均平动动能:
- 理想气体状态方程:
- 理想气体压强公式:
- 考点10:理想气体内能:
- 理想气体内能只是温度的单值函数,理想气体处于平衡装填,具有确定的内能
考试快速做题指南
不要写成 - 要看清楚题目问的是 平均平动动能 还是 平均动能(平动+转动)
- 针对单个分子:平均平动动能 和 平均动能(平动+转动)
- 针对全体分子:内能






麦克斯韦速率分布函数(考点11)
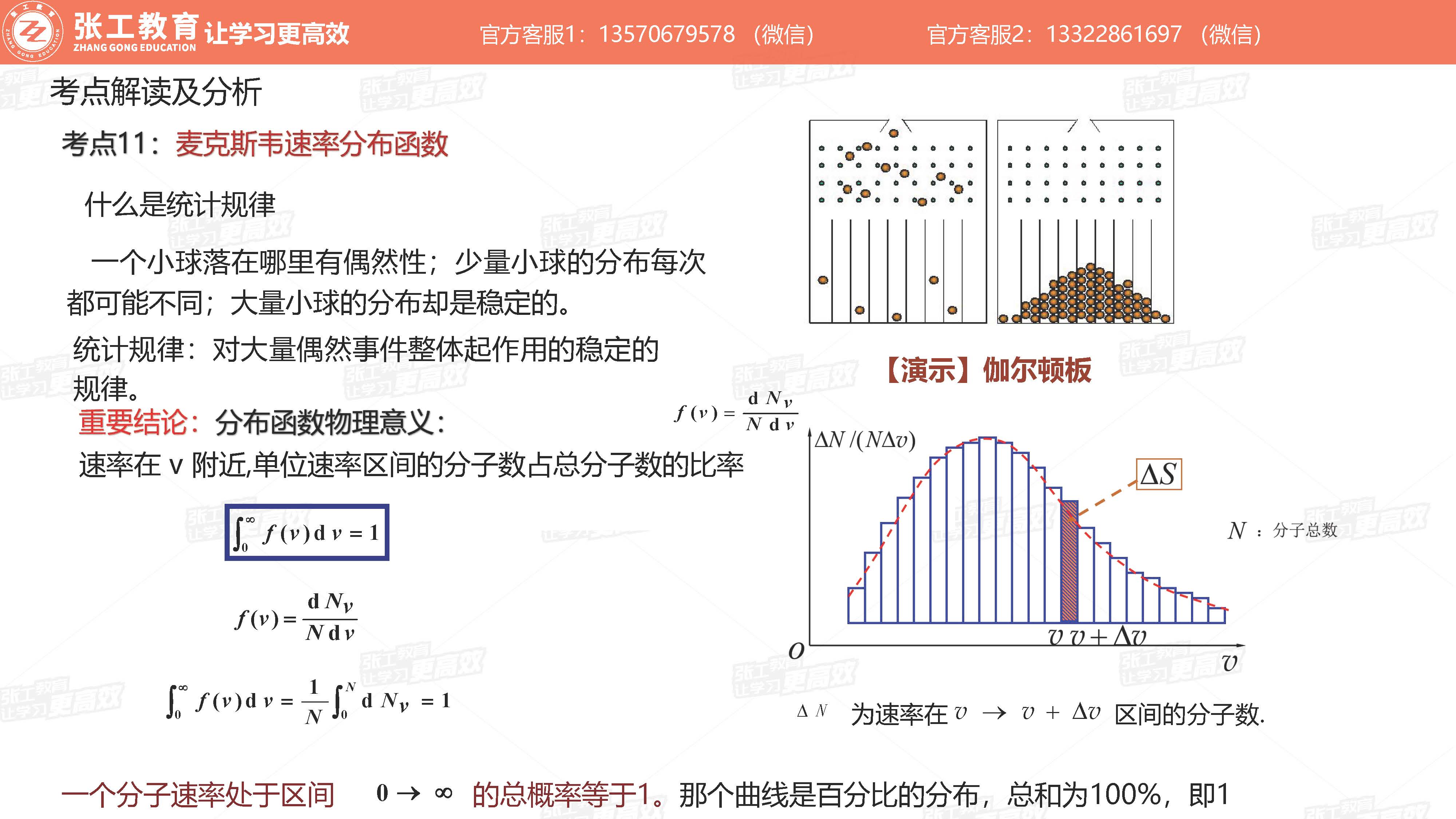
- 什么事统计规律
- 分布函数的图像
- x坐标表示速率
- y坐标表示百分数(概率密度、单位速率区间的分子数占总分子数的比率)
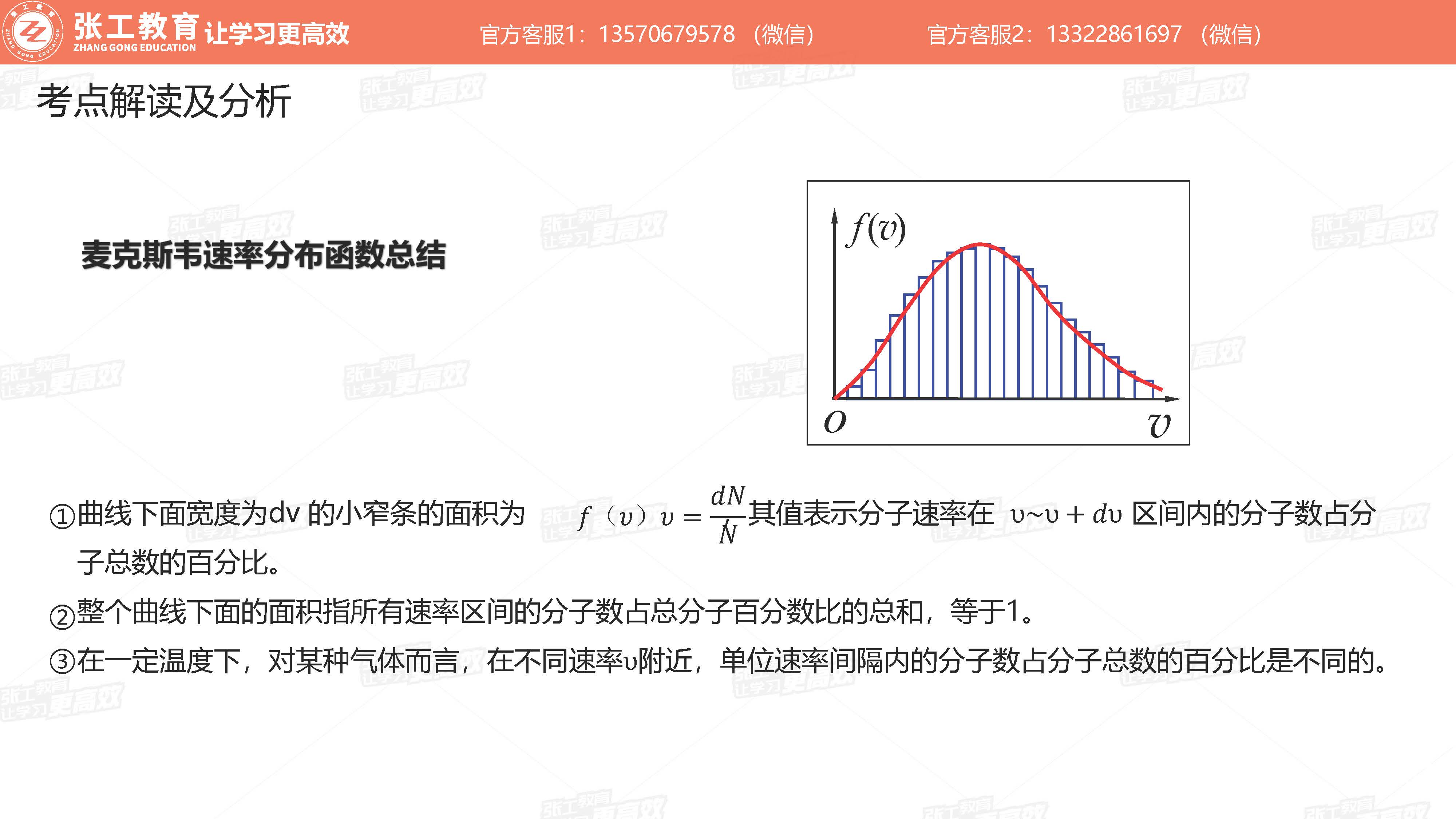
- 小窄条面积意义
- 分布函数的图像与x轴围成面积为1,即100%
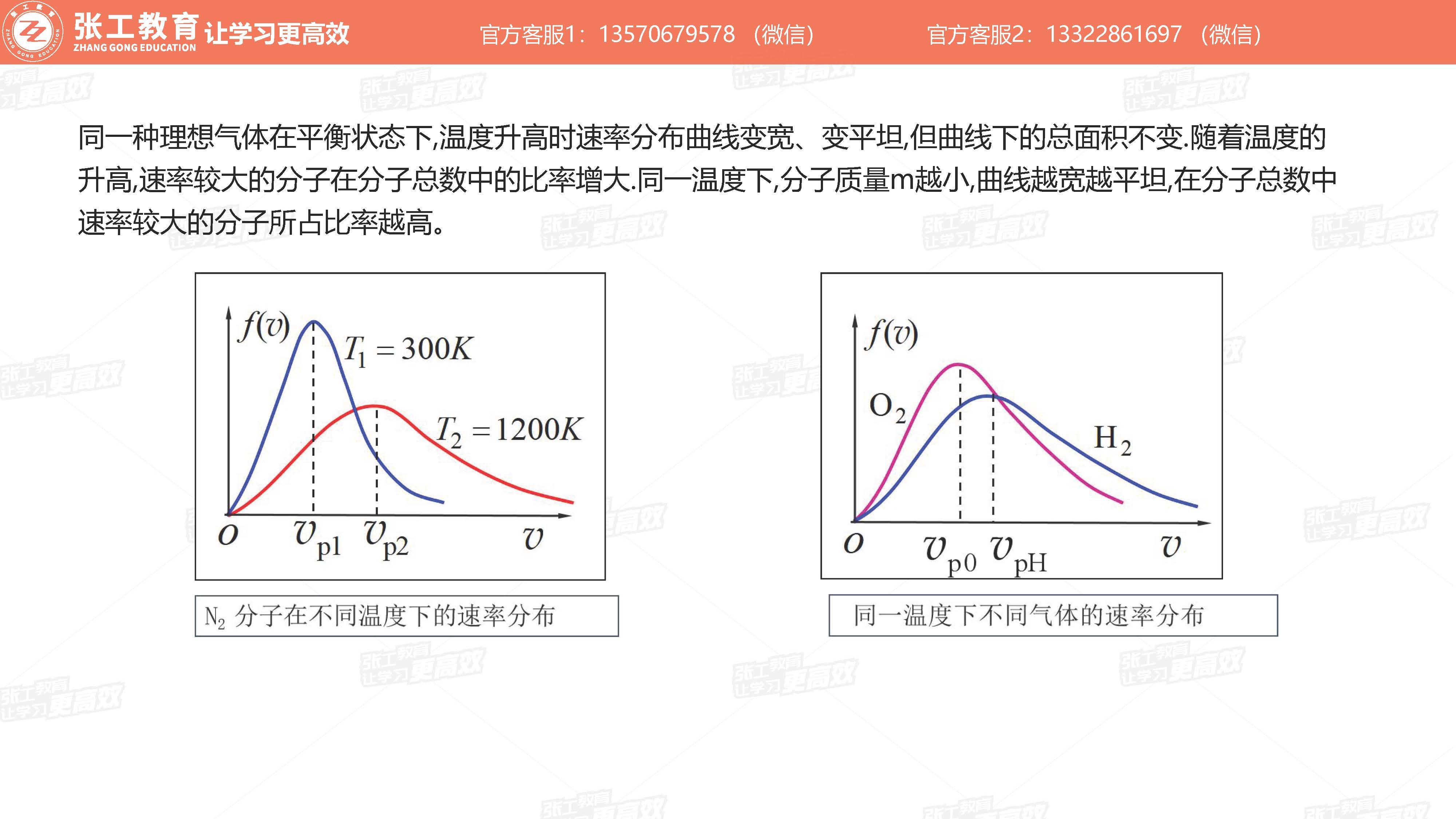
- 温度越高、分子质量越小:图像越平坦、速率较大的分子占比越高
- 不同速率附近的分子数百分比不同
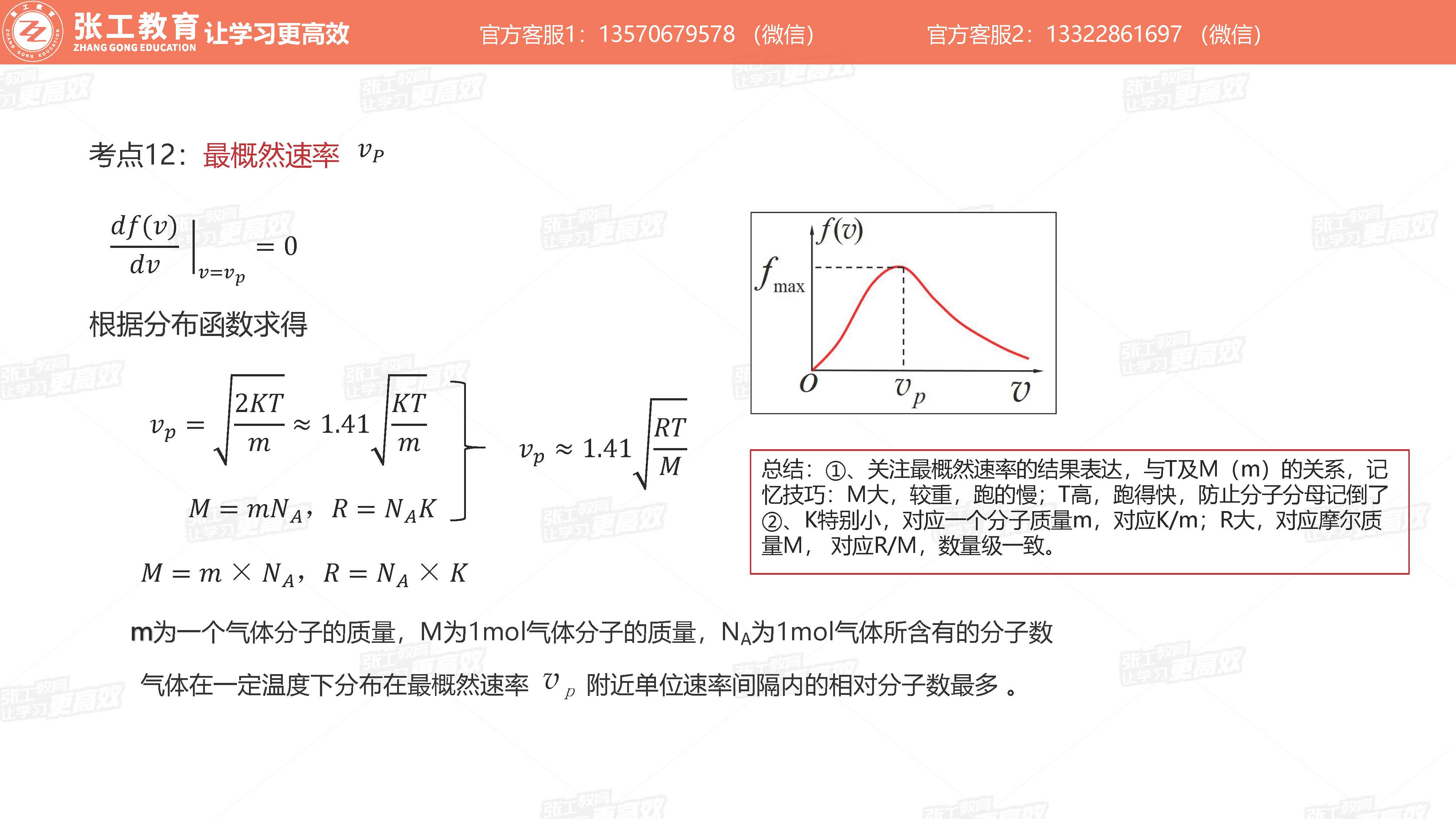
- 最概然速率及其物理意义
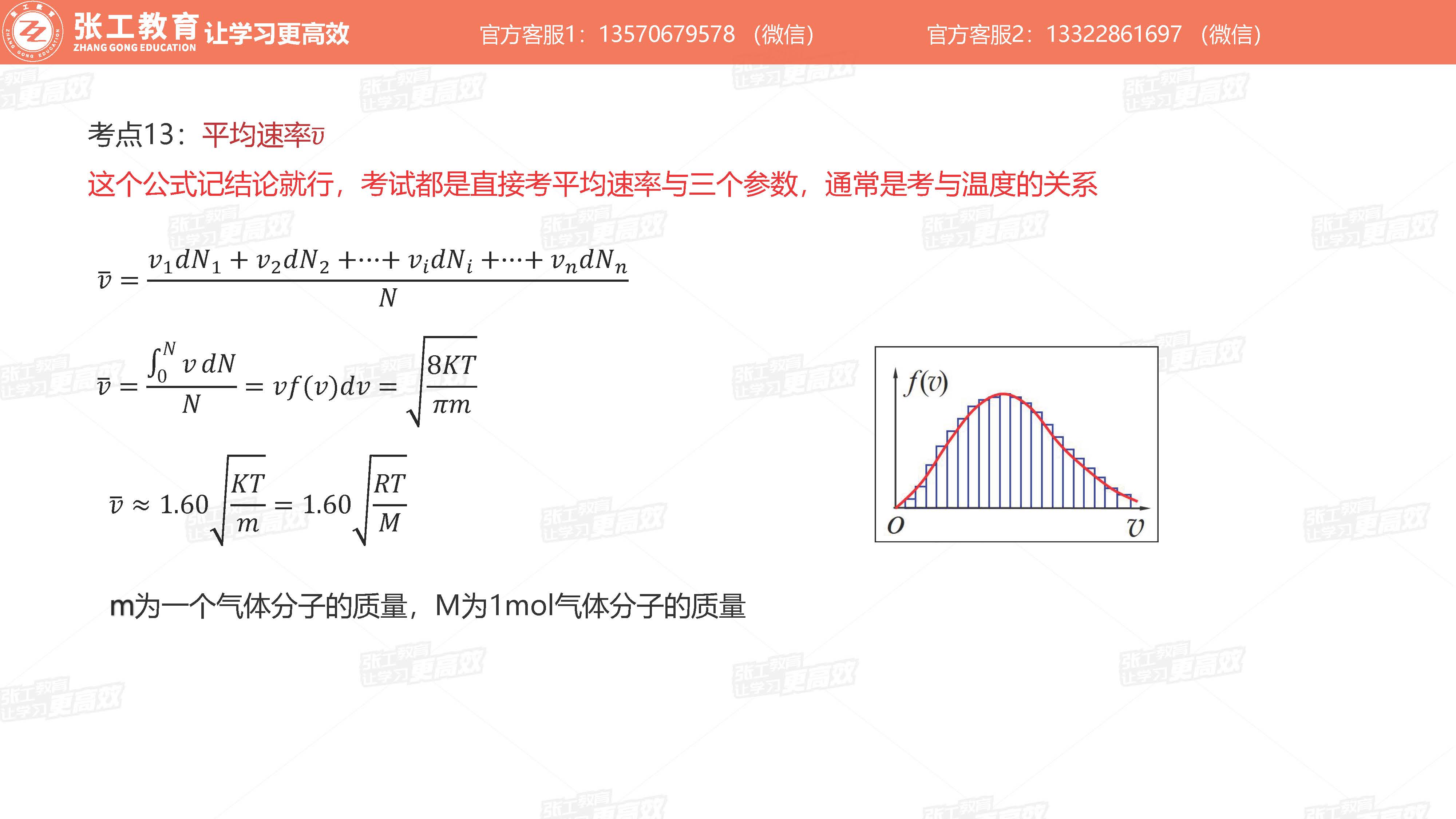
- 平均速率
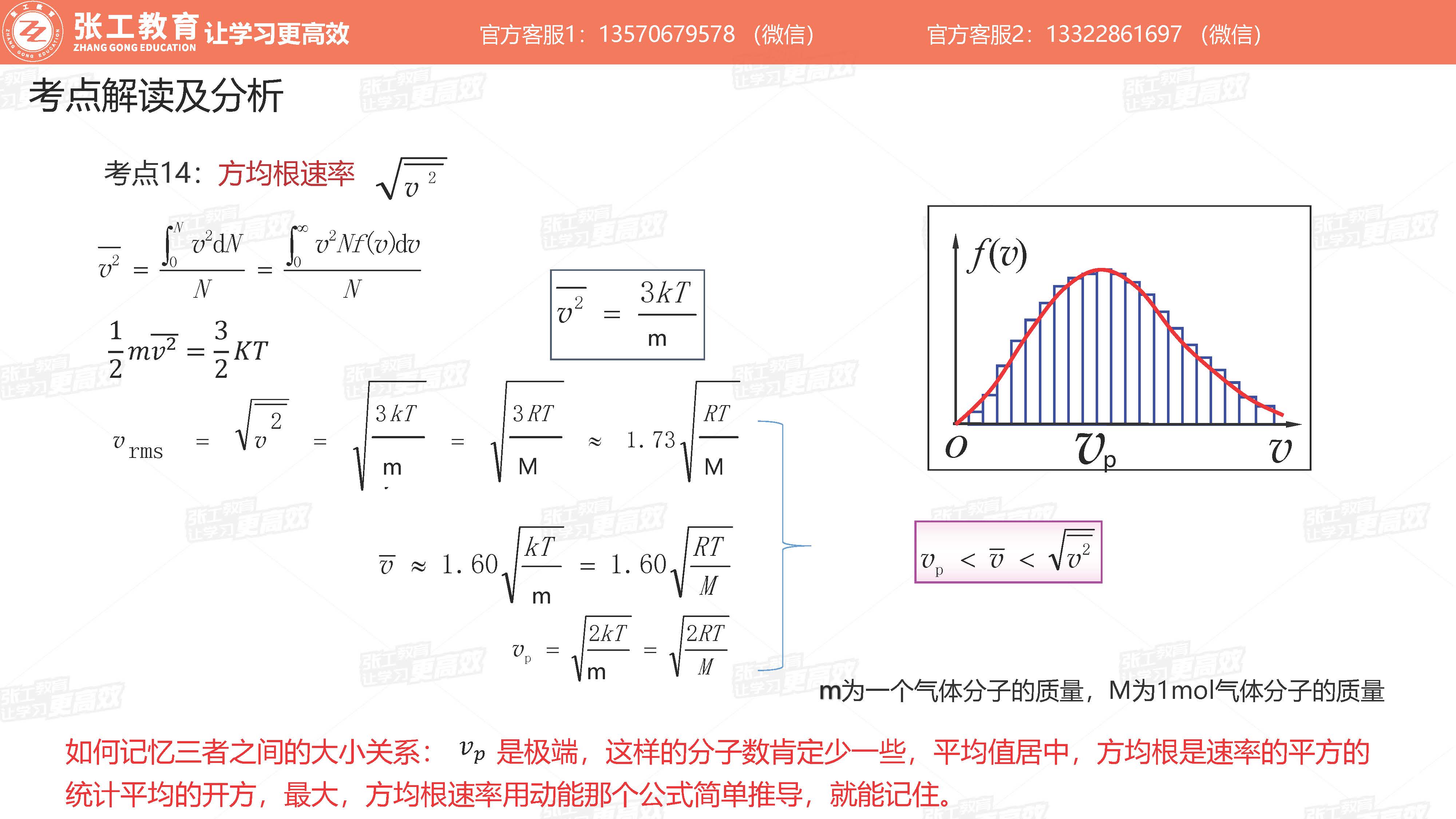
- 方均根速率
三种速率的关系(上述公式中:m是一个分子的质量,M是1mol分子的质量)
三种速率结论及应用范围
- 三种速率均与
成正比,与 成反比 - 讨论速率分布用:
- 计算分子平均平动动能用:
- 讨论分子的碰撞频率用:
- 三种速率均与
麦克斯韦速率分布函数的物理意义
最概然速率
平均速率
方均根速率
三种速率的重要结论及应用范围
麦克斯韦速率分布函数总结(3点)

平均碰撞频率和平均自由程(考点15)
- 自由程:分子两次碰撞之间所经过的直线路程
- 分子平均自由程
:自由程的统计平均值 - 平均碰撞频率
:单位碰撞的平均次数(统计平均值) - 平均碰撞频率与分子大小、分子密度、平均速率的关系
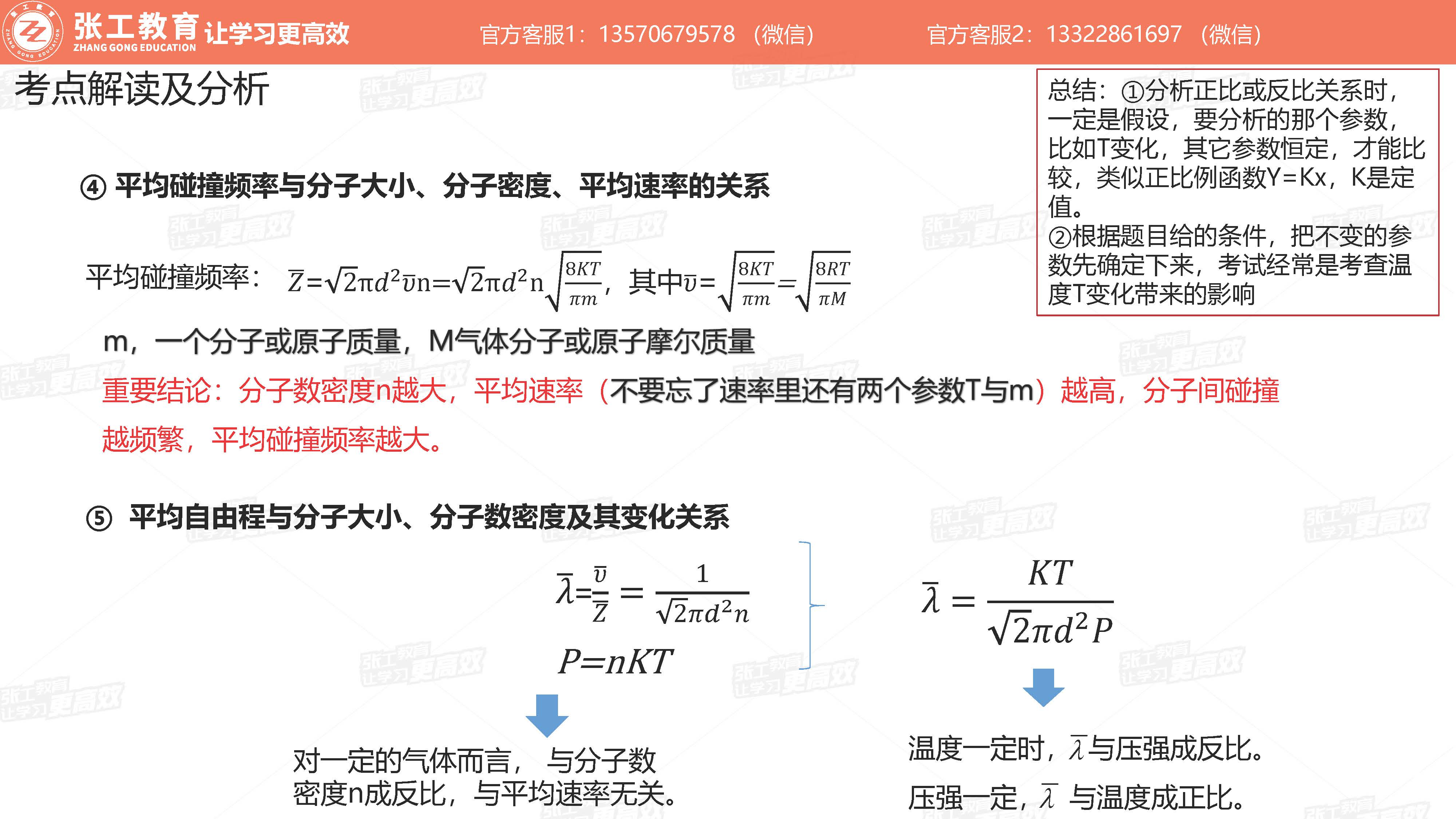
- 重要结论:分子数密度n越大,平均速率
越高,分子间碰撞约频繁,平均碰撞频率越大
- 重要结论:分子数密度n越大,平均速率
- 平均自由程与分子大小、分子数密度及其变化关系
- 对于一定的气体而言,与分子数密度成反比,与平均速率无关
- 温度一定,与压强成反比
- 压强一定,与温度成正比

热力学第一定律(考点16)
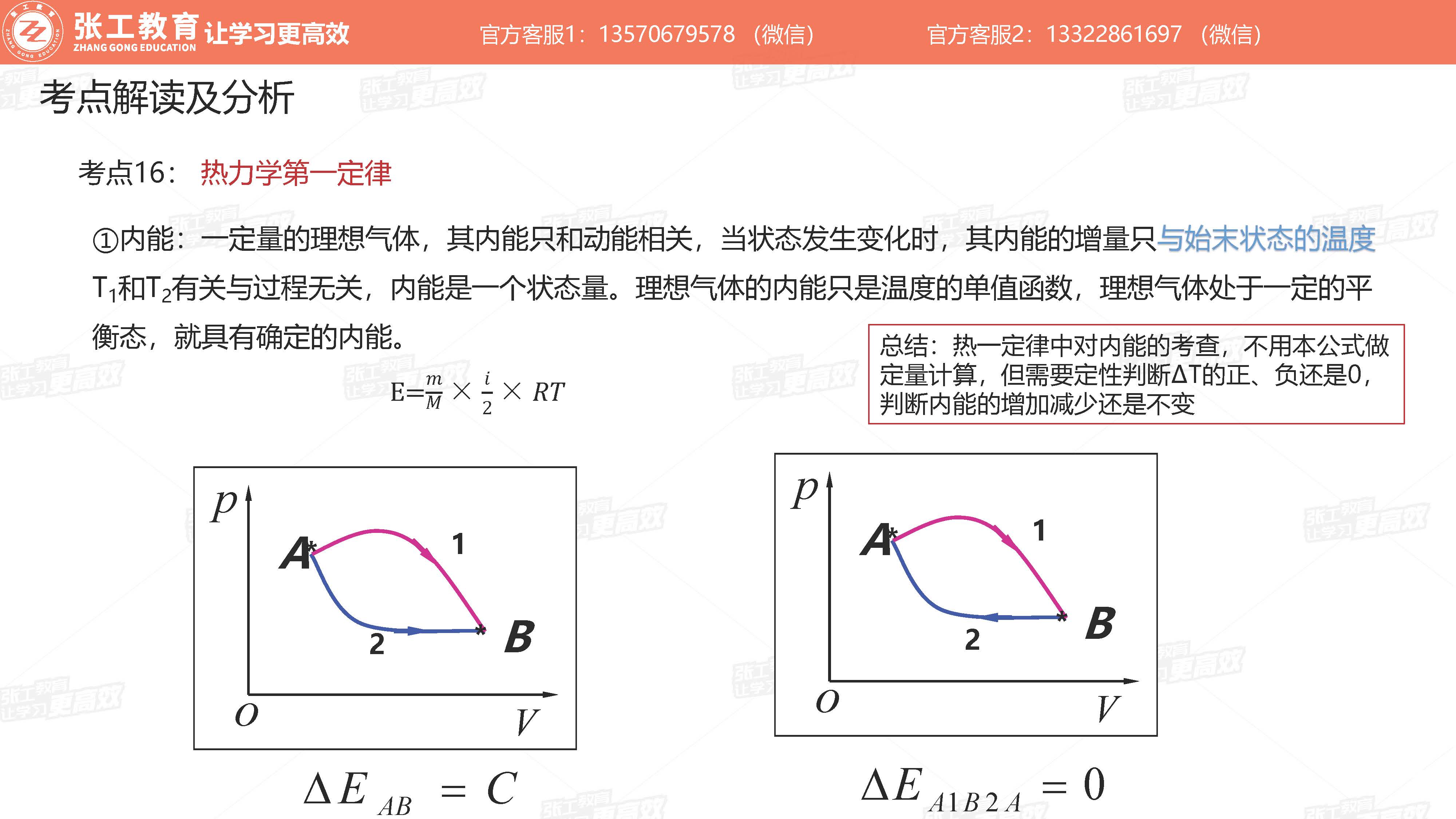
内能
- 只与始末状态的温度有关,与过程无关,内能是一个状态量
- 不需要定量计算,只需要根据
的正、负、0判断内能的增加还是不变
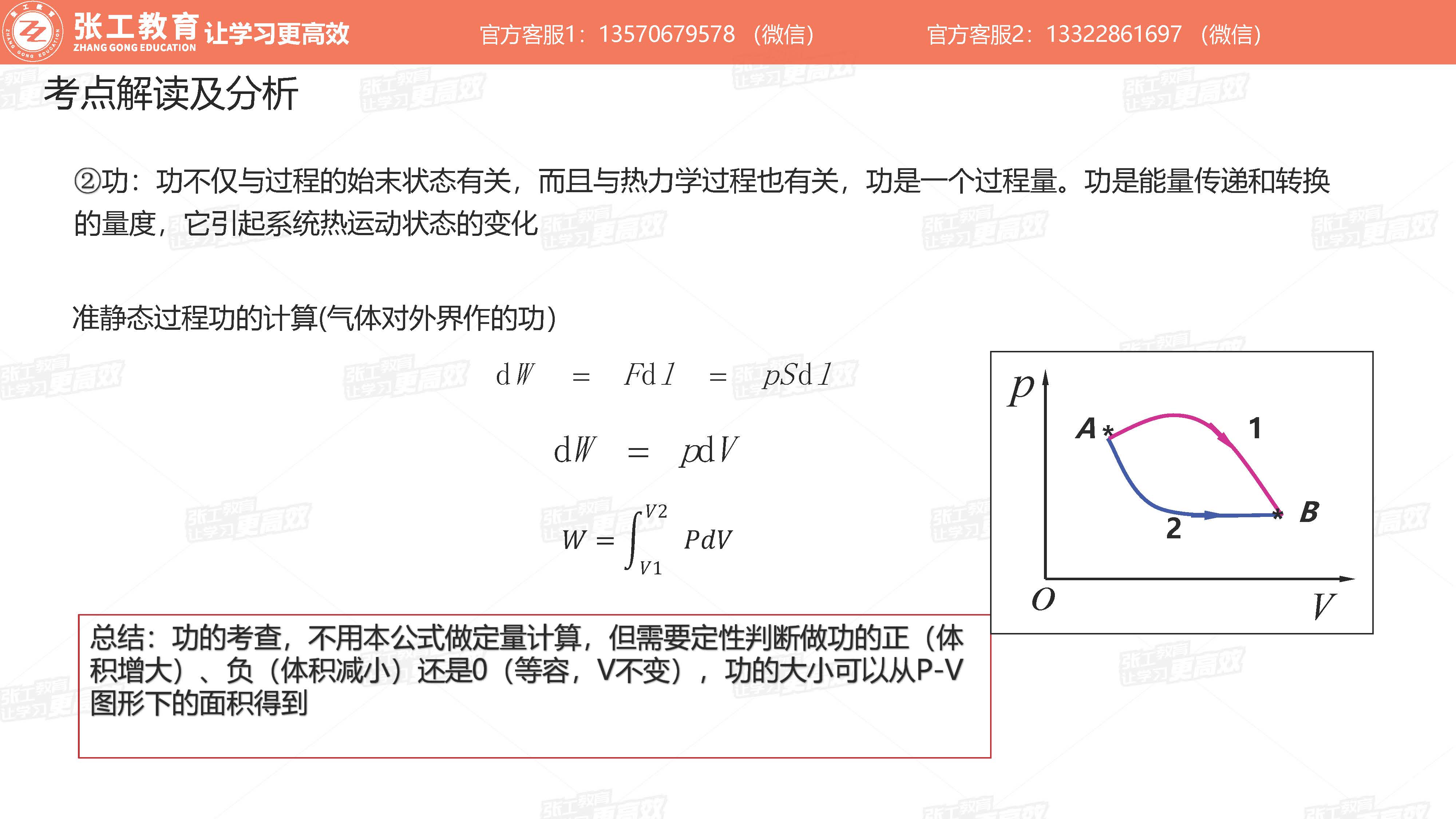
功
- 不仅与始末状态有关,而且与热力学过程有关,功是一个过程量
- 不需要定量计算,但需要定型判断做功的正(体积增大)、负(体积减小)、0(等容,V不变),功的大小可以从P-V图形下的面积得到
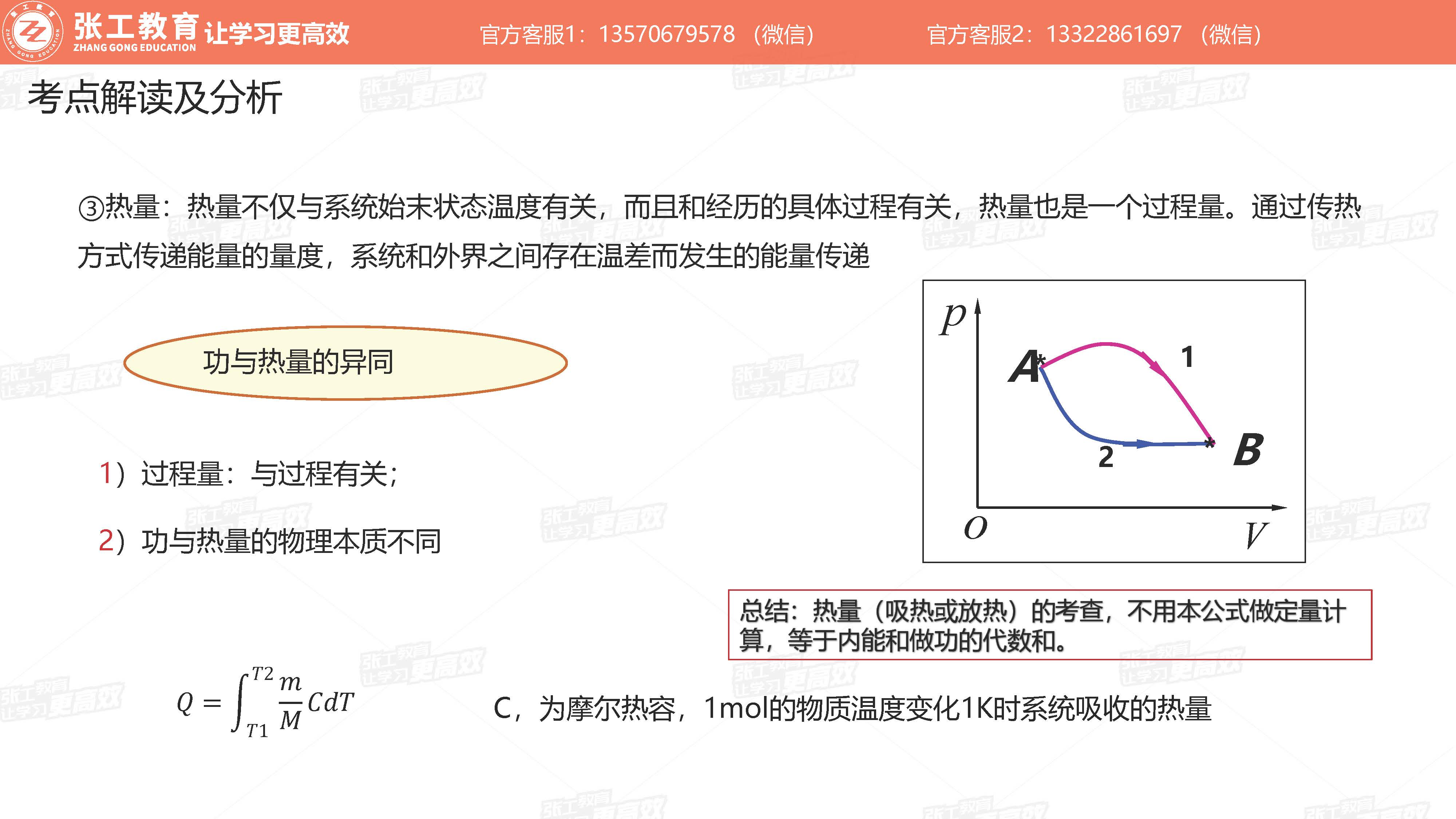
热量
- 不仅与始末状态温度有关,而且与热力学过程有关,功是一个过程量。通过传热方式传递能量的量度,系统与外界之间存在温差而发生的能量传递。
- 热量(吸热或放热)的考察,不用本公式做定量计算,等于内能和做功的代数和。
- 功与热量的物理本质不同
热力学第一定律
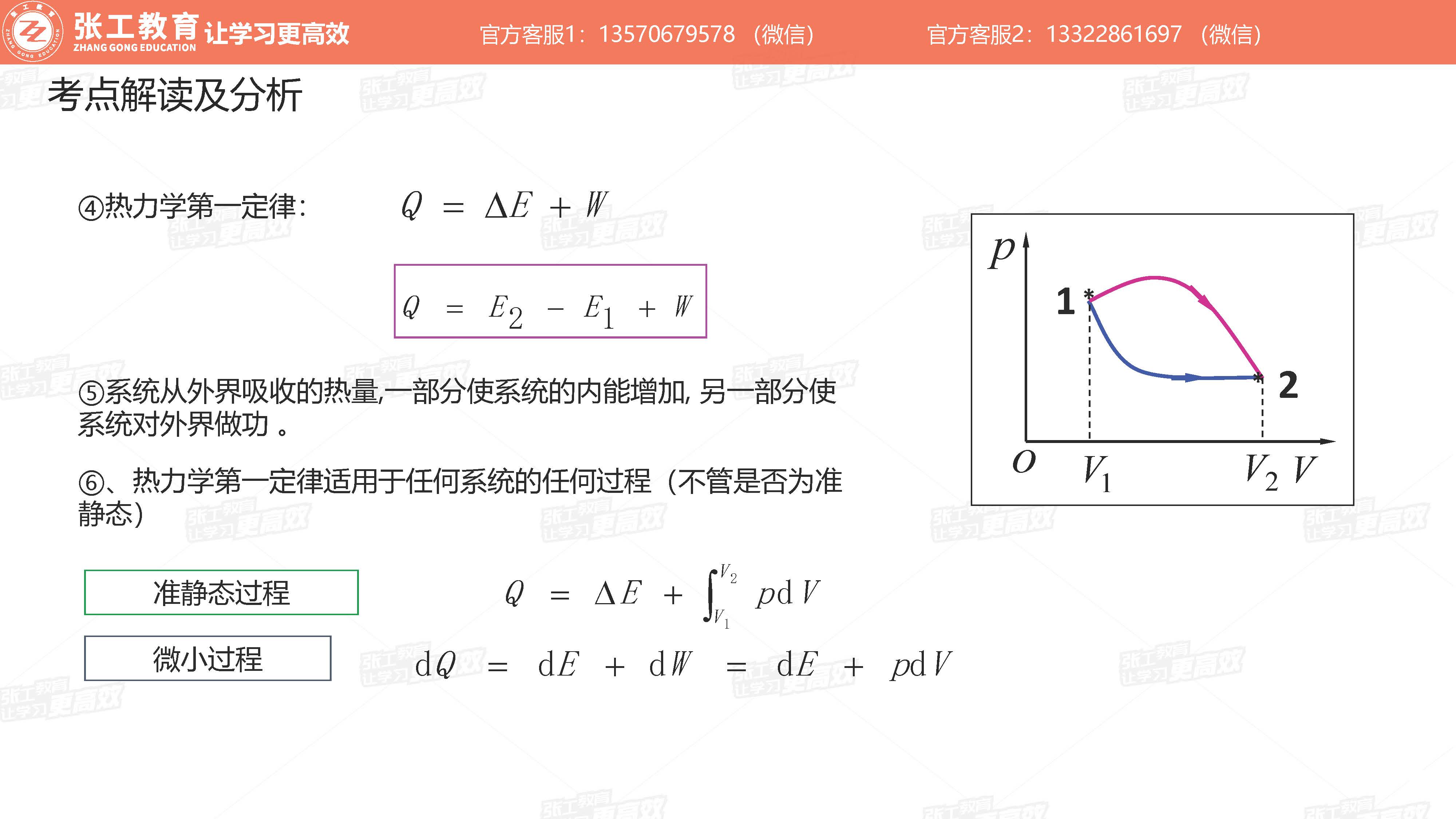
- 系统从外界吸收的热量,一部分使系统的内能增加,另一部分使系统对外界做功。
- 适用于任何系统的任何过程(不管是否为准静态)
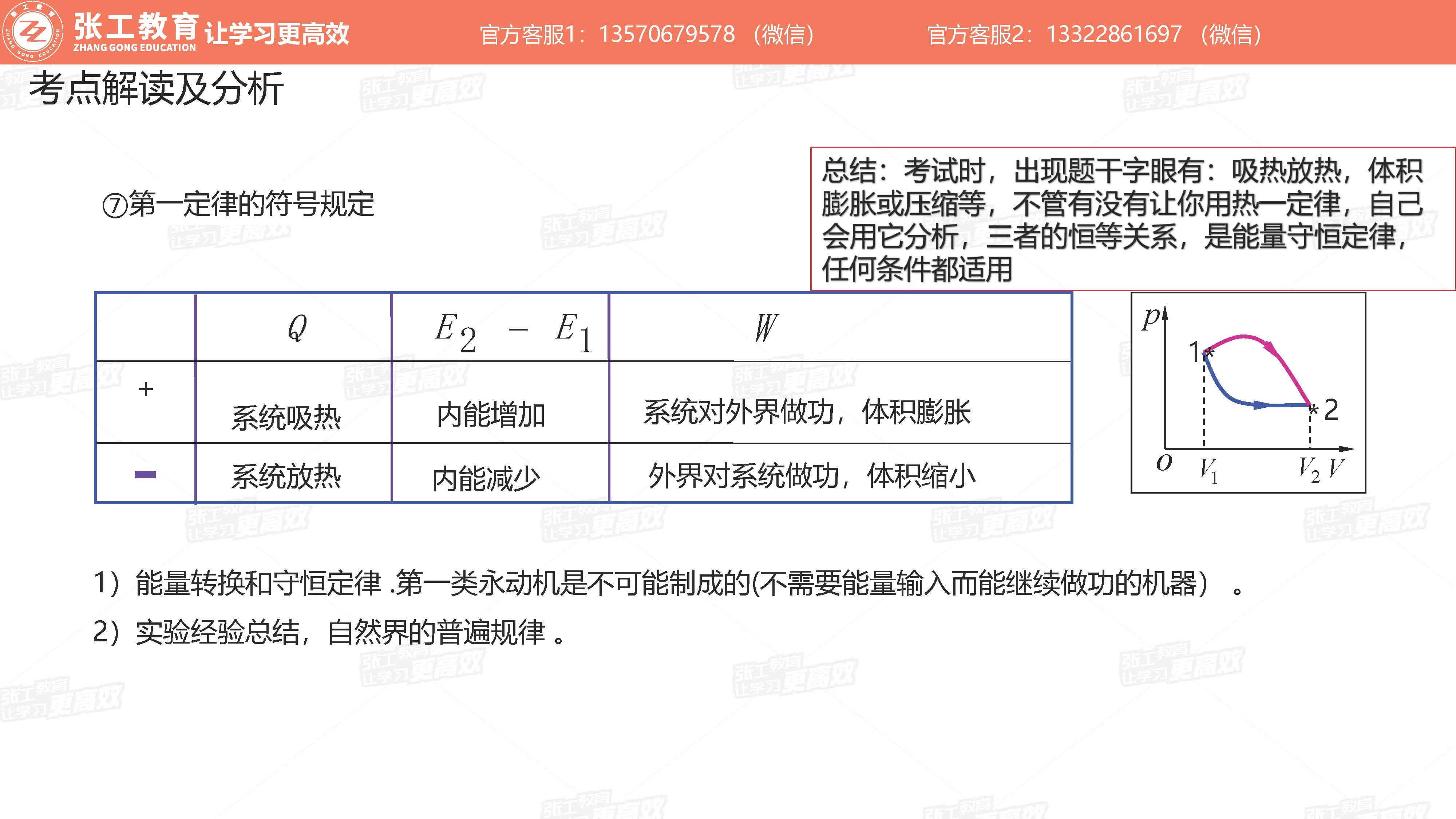
热力学第一定律符号规定
符号 Q W + 系统吸热 内能增加 系统对外界做功(体积膨胀) - 系统放热 内能减少 外界对系统做功(体积缩小)
热力学2
等体过程(考点1)
- 外界传递给系统的热量,全部用来增加气体的内能(温度变化),不做功。
- 系统的内能增量 = 吸热
- 定容摩尔热熔:
INFO
- 想象一下高压锅烧开水,内部压强升高、温度升高、体积不变。

等压过程(考点2)
- 系统与外界交换的热量,一部分用来改变内能,另一部分用来做功,具体分析过程,全部根据理想气体状态方程和热一定律
- 系统吸热 = 内增增量 + 做功
- 定压摩尔热容:

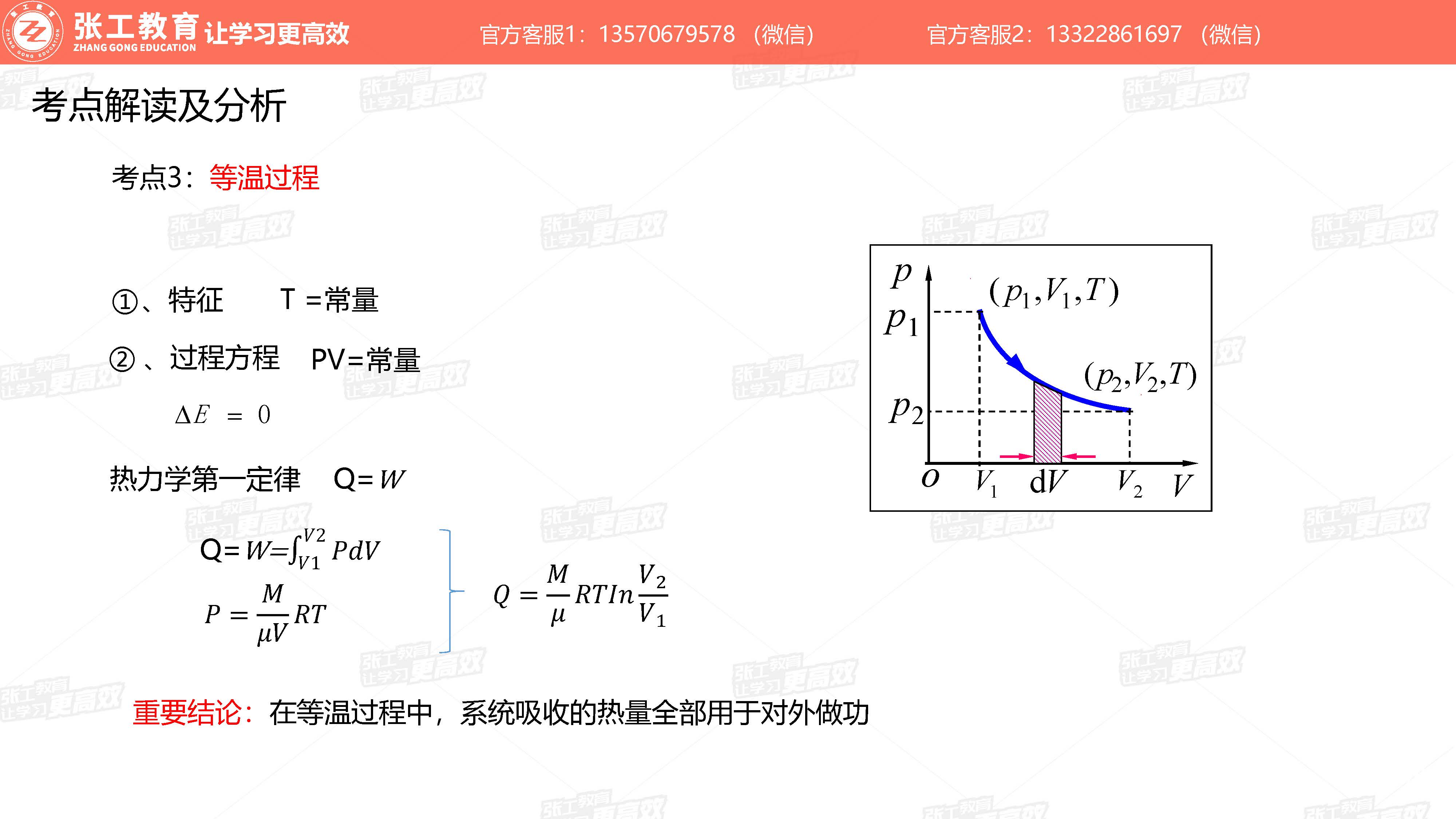
等温过程(考点3)
- 在等温过程中,系统吸收的热量全部用于对外做功。
- 系统吸热 =
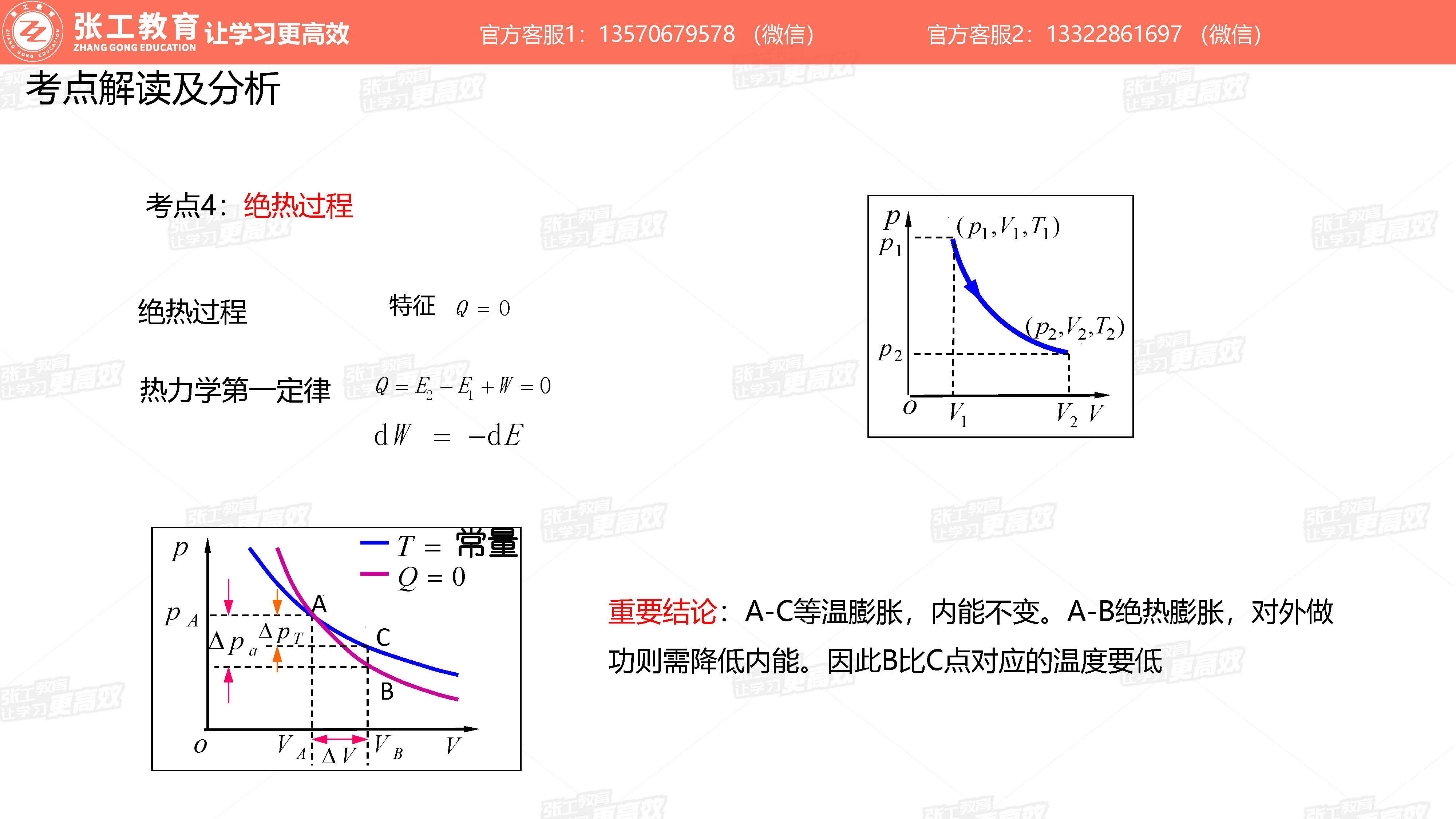
绝热过程(考点4)
- 在绝热过程中,对外做功则需降低内能。
INFO
- 想象一下普通的锅烧开水,锅盖被顶开,压强不变,温度升高,体积增大。
和 的公式一定要记清楚,考试重点 - 等体、等压这类题的出题方向就是反复利用理想气体状态方程的两种形式进行反复变换。
- 等温、绝热过程的分析一定要使用P-V图像来分析。
循环过程(考点5)
- 热机:利用循环过程,持续地将热量转变为做功的机器
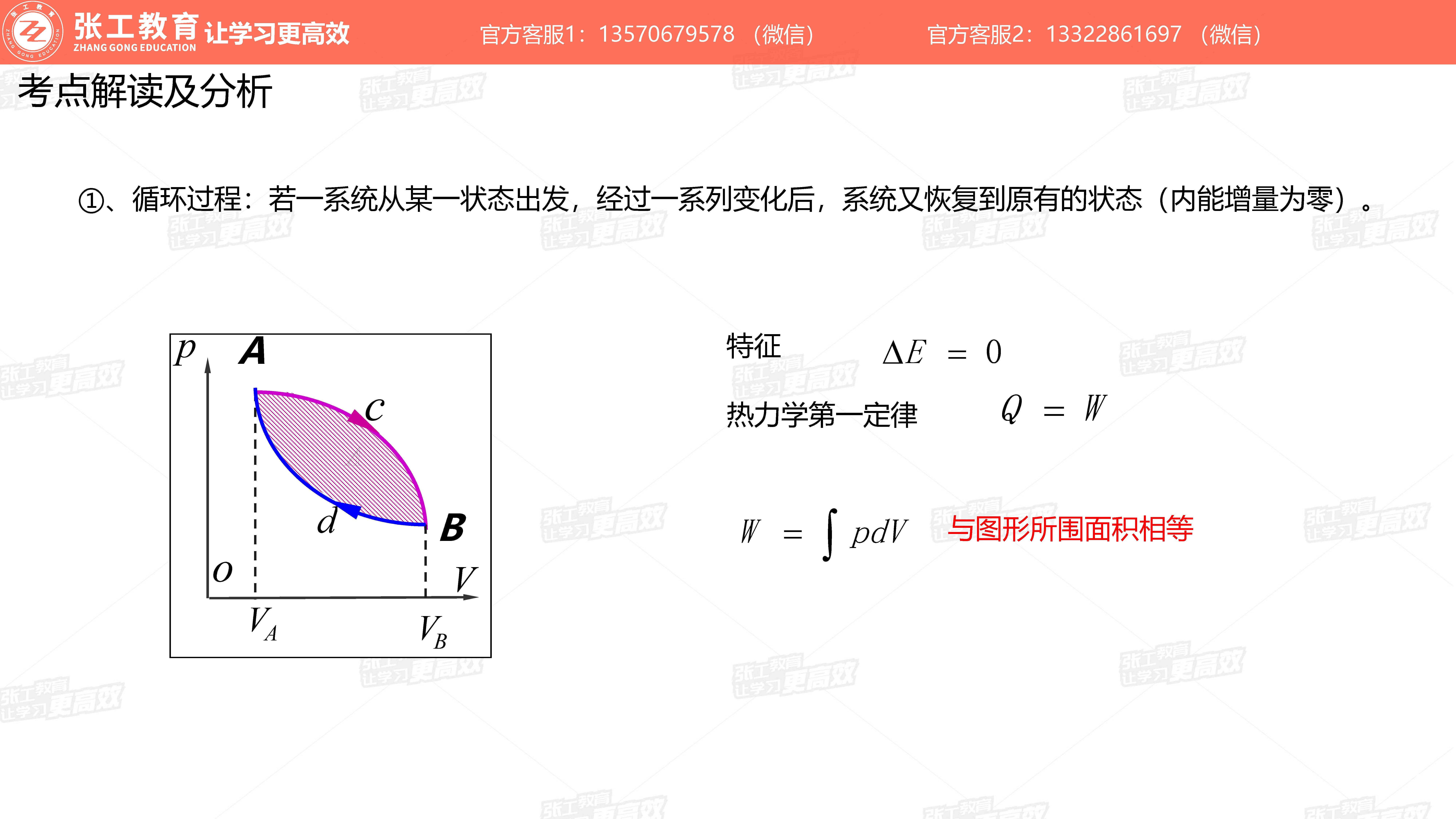
- 循环过程
- 一个系统从某一状态出发,经过一系列变化后看,系统又恢复到原有的状态。
- 内能增量为零。
- 热力学第一定律:
- W与图形所围面积相等
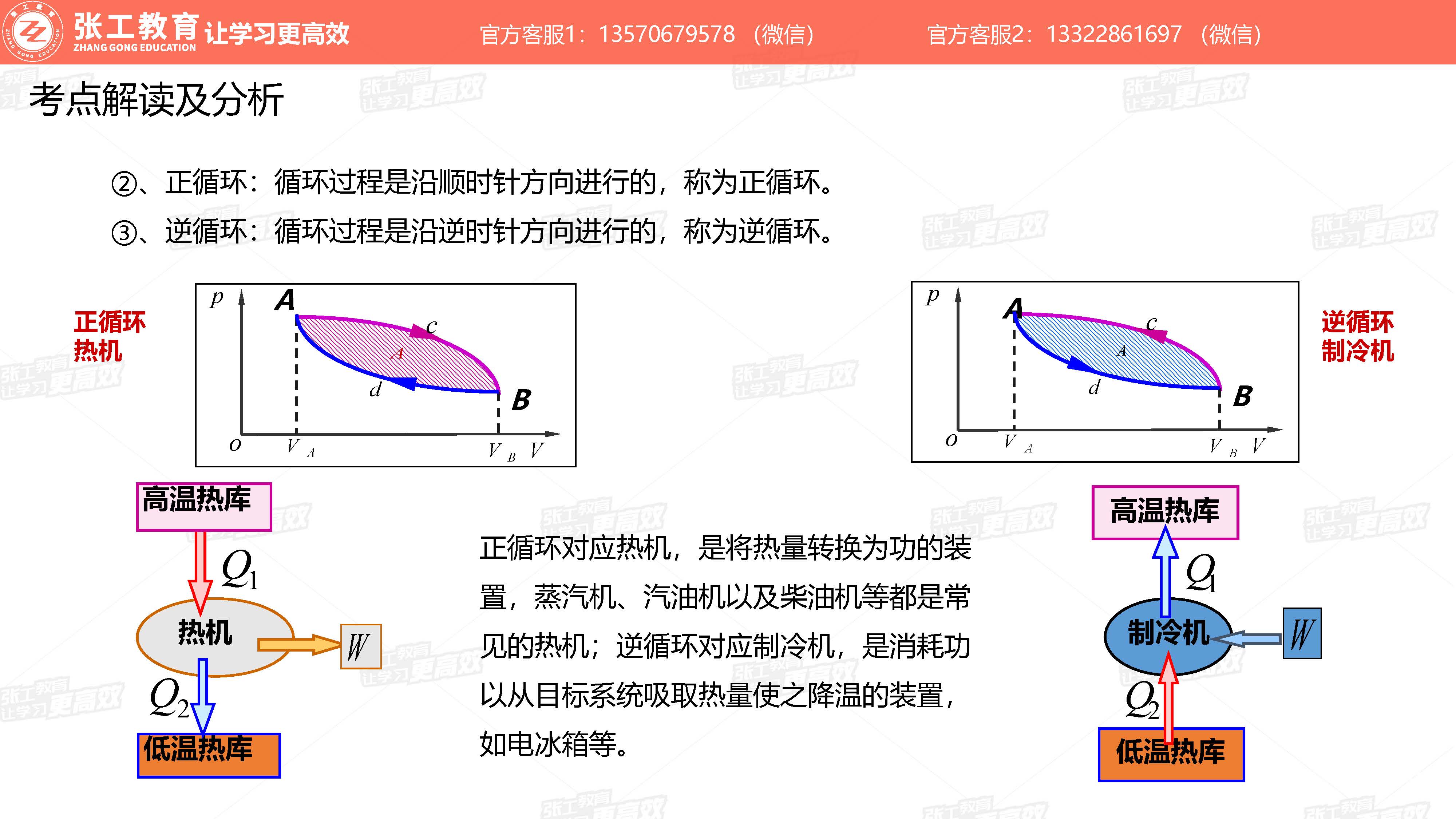
- 正循环:循环过程是沿顺时针方向进行的(蒸汽机、汽油机、柴油机)
- 逆循环:循环过程是沿逆时针方向进行的(制冷机)
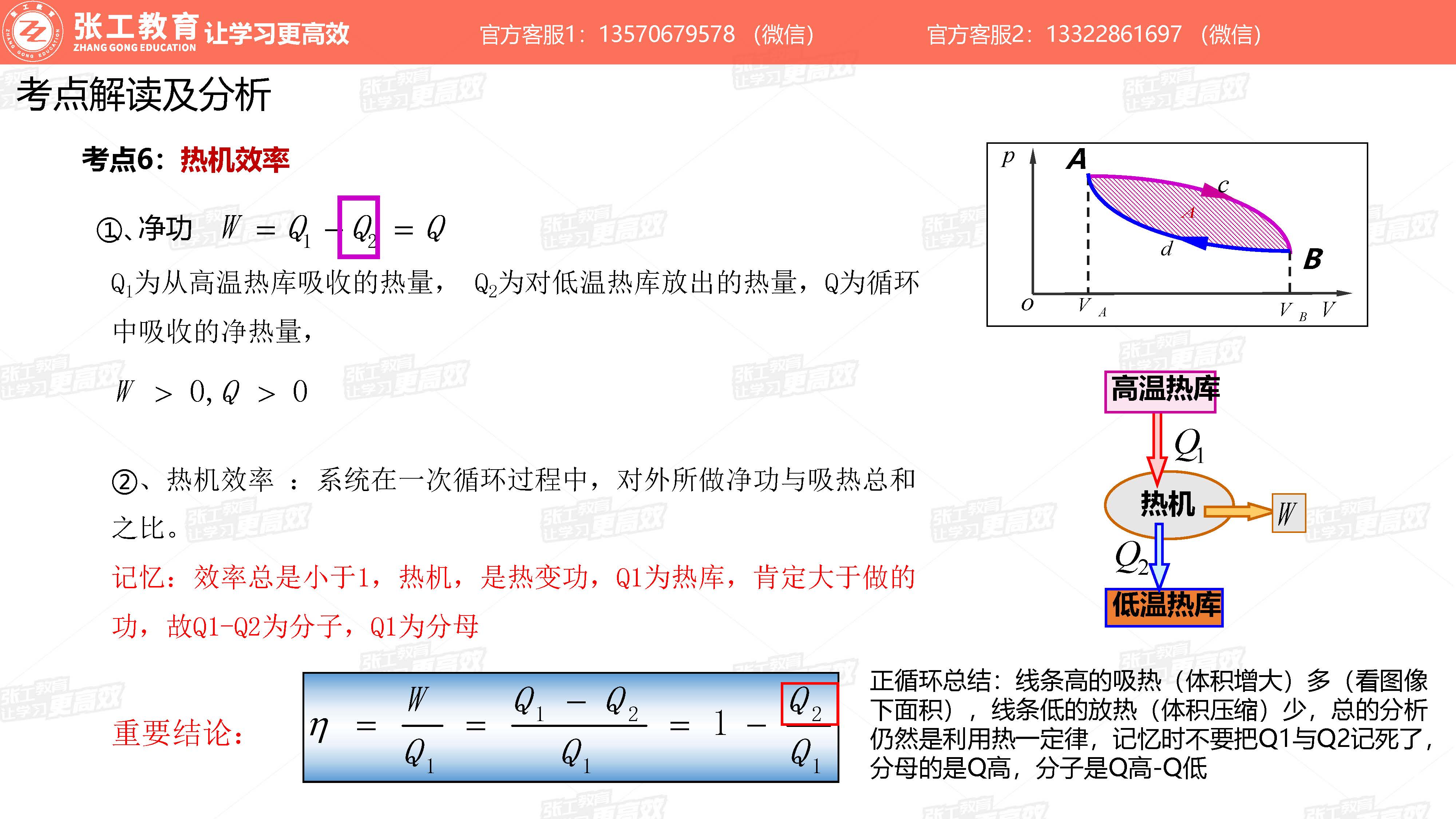
热机效率(考点6)
- 热机效率:对外作功与吸热总和之比
- 重要结论:
考试快速做题指南
- 线条高的吸热(体积增大),线条低的放热少(体积压缩),
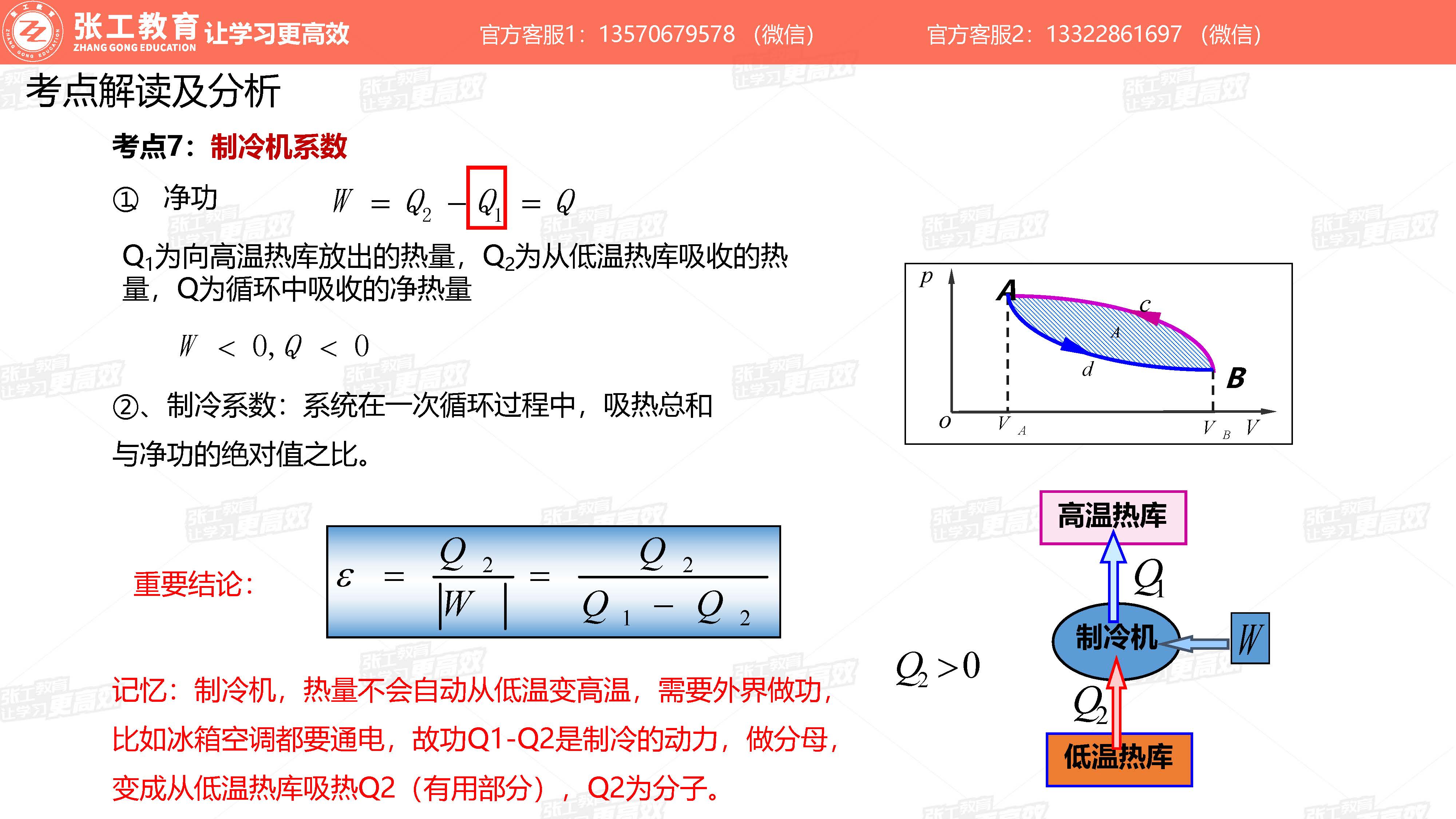
制冷机效率(考点7)
- 制冷效率:系统在一次循环过程中,吸热总和与净功的绝对值之比
- 重要结论:
- 净功 =
考试快速做题指南
- 制冷机,热量不会自动从低温变高温,需要外界做功

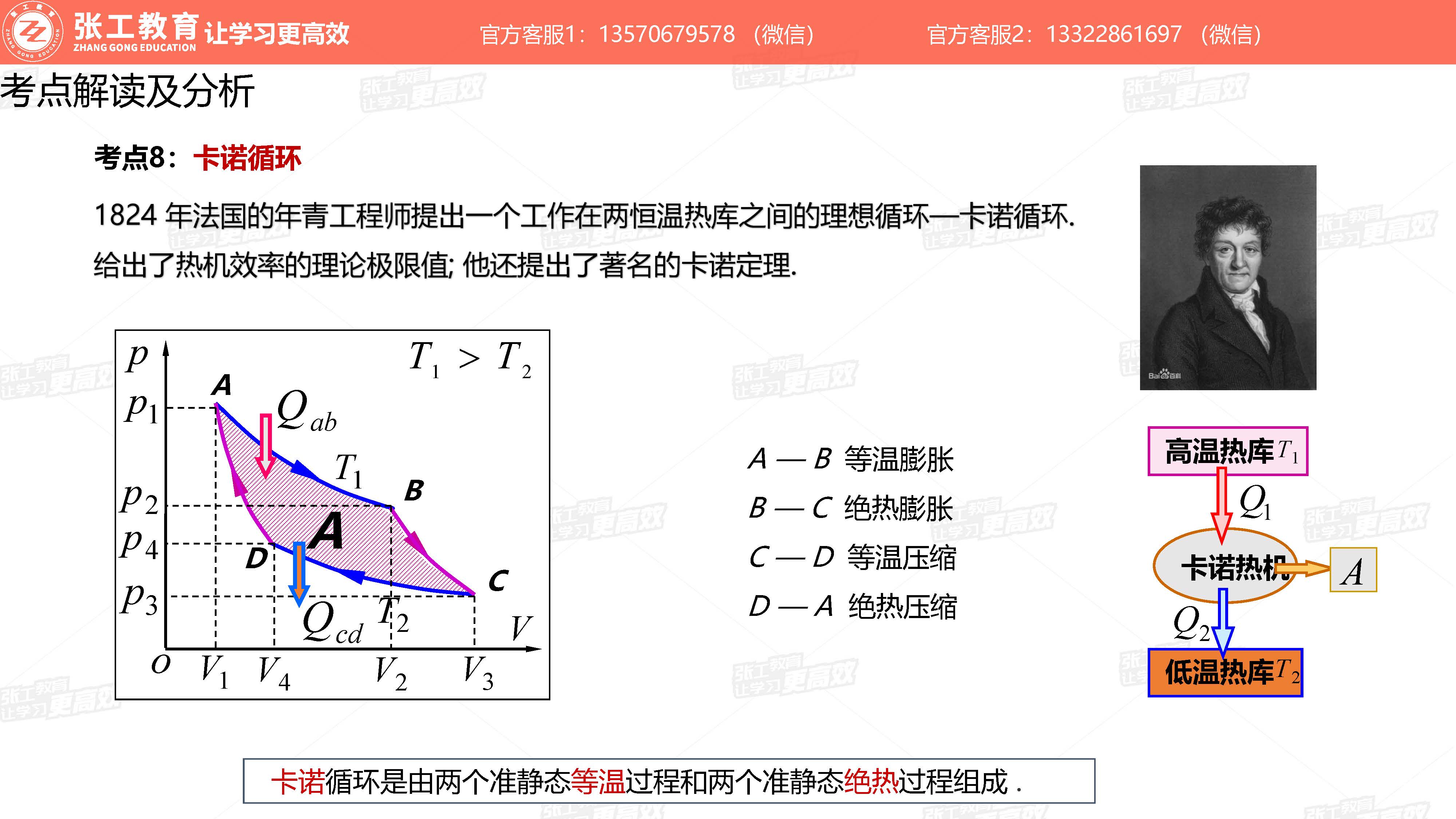
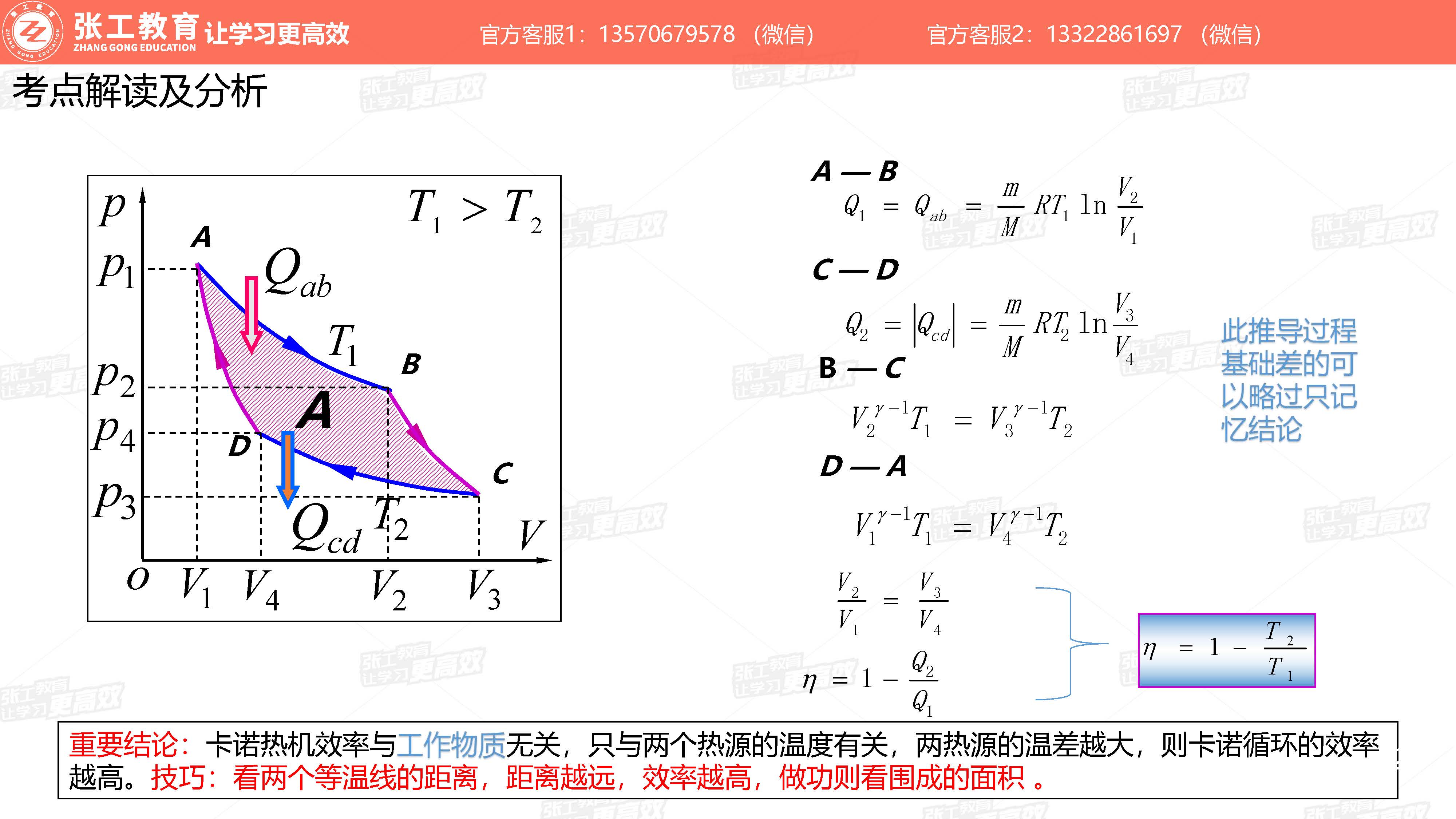
卡诺循环(考点8)
卡诺热机效率与工作物质无关,只与两个热源的温度有关,两热源的温差越大,则卡诺循环的效率越高。看两个等温线的距离,距离越远,效率越高,做功则看围成的面积。
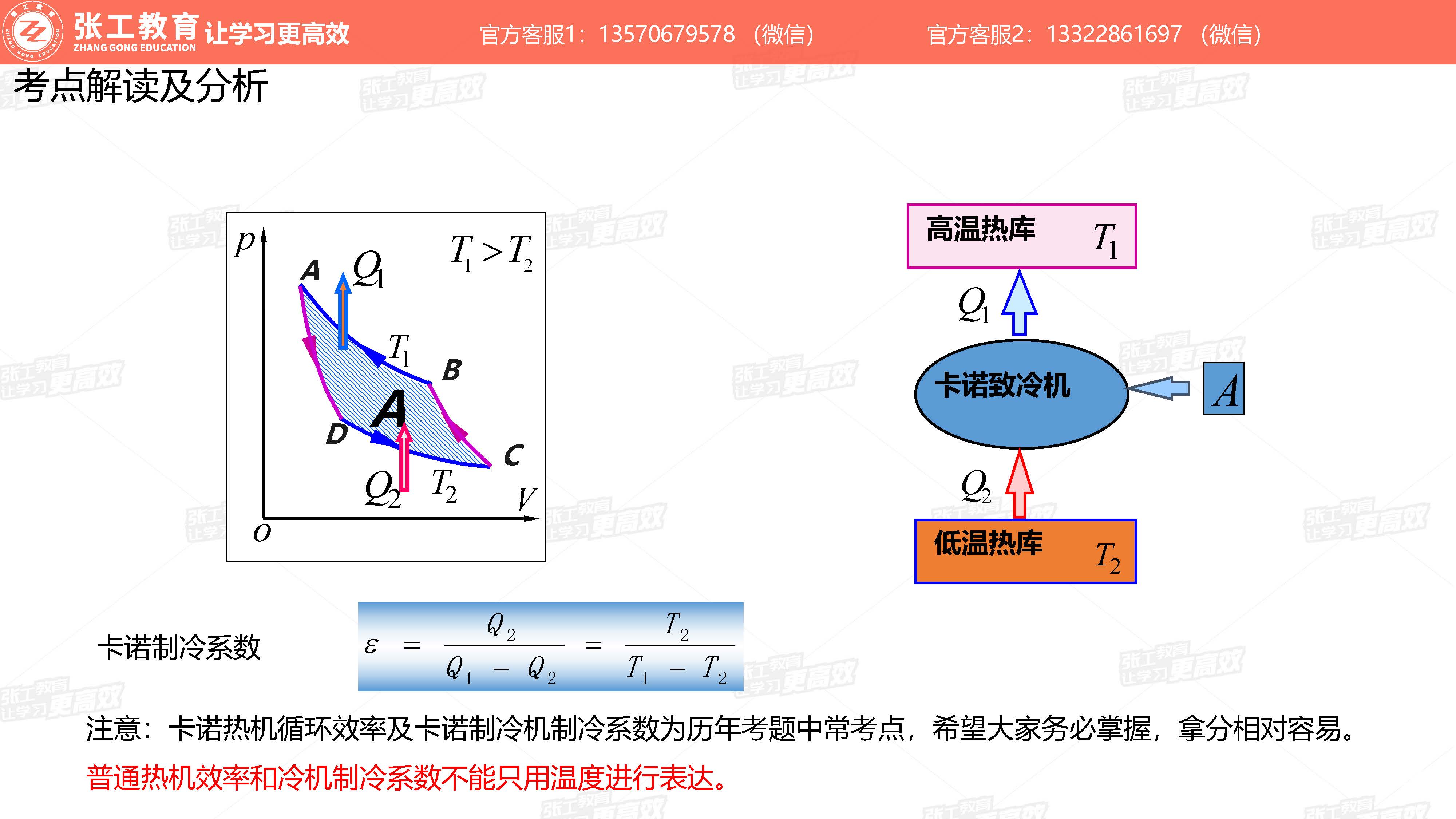
卡诺制冷系数
考试快速做题指南
- 卡诺循环两个绝热曲线与x轴围成的面积相等,二者做功大小相等、方向相反。
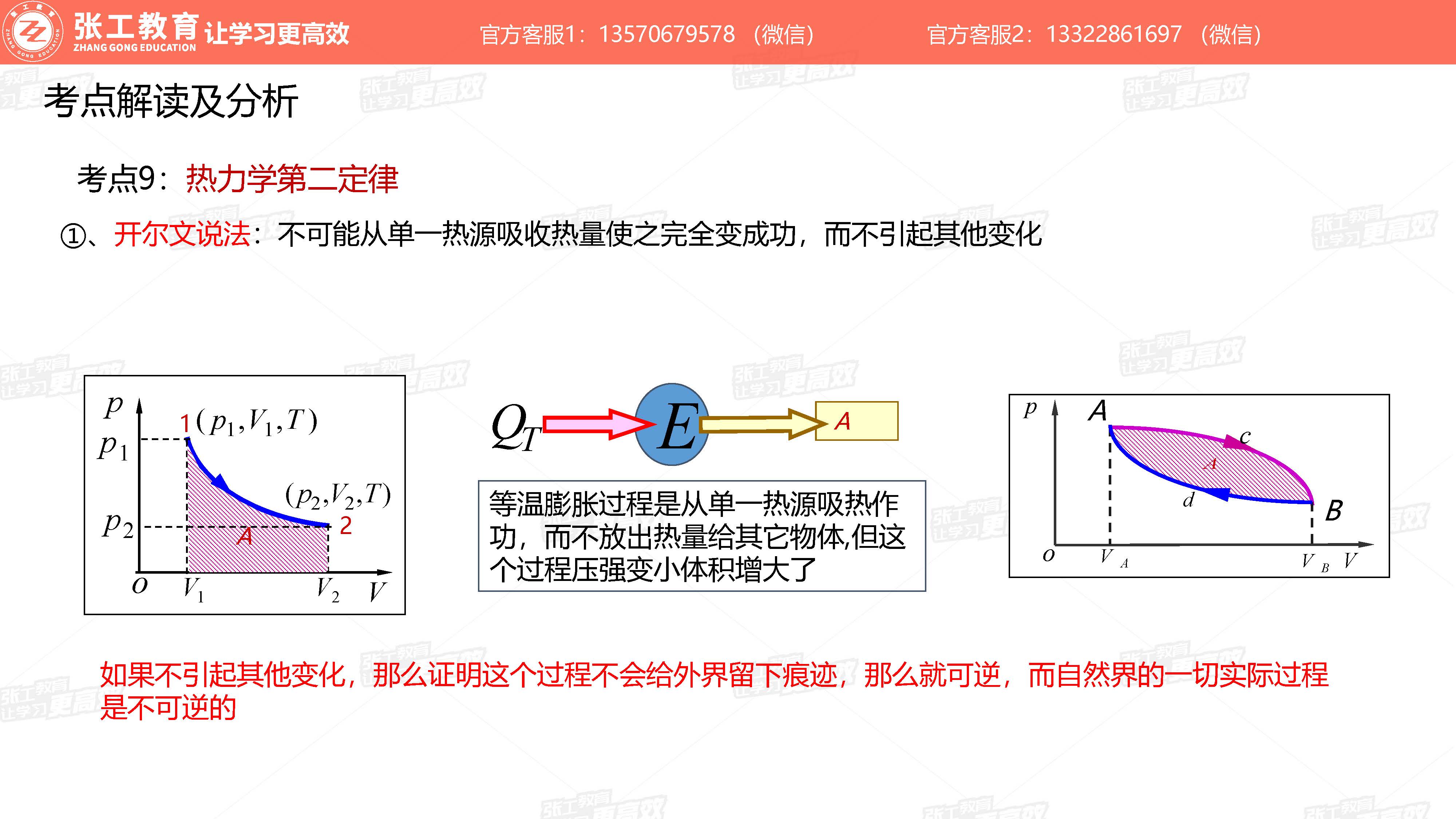
热力学第二定律(考点9)
- 开尔文说法:不可能从单一热源吸收热量使之完全变成功,而不引起其他变化
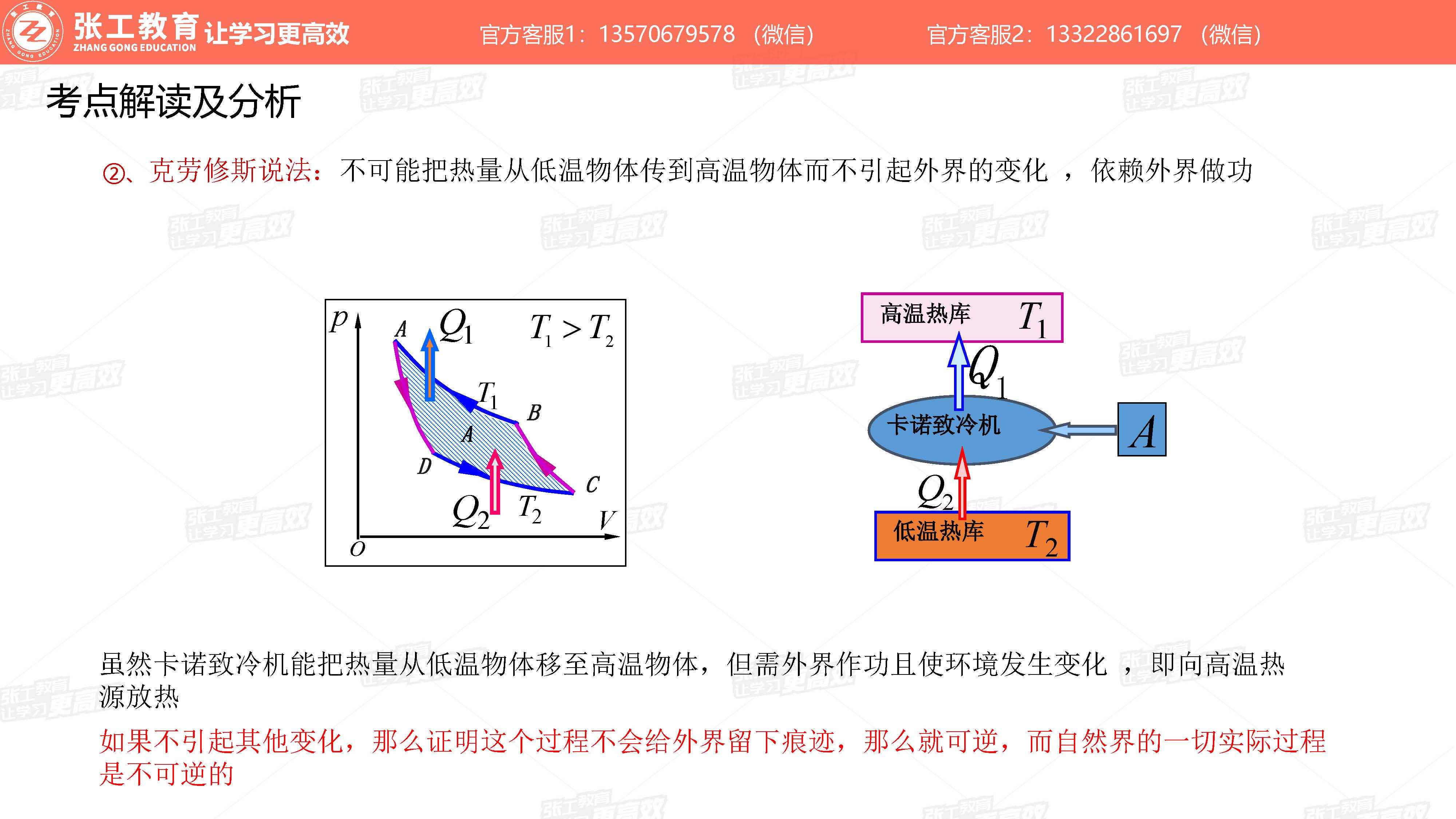
- 克劳修斯说法:
- 热力学第二定律几点说明
- 可逆过程和不可逆过程
- 功热转换不可逆举例、热传导不可逆举例
- 气体的绝热自由膨胀
- 热力学第二定律小结(4点)





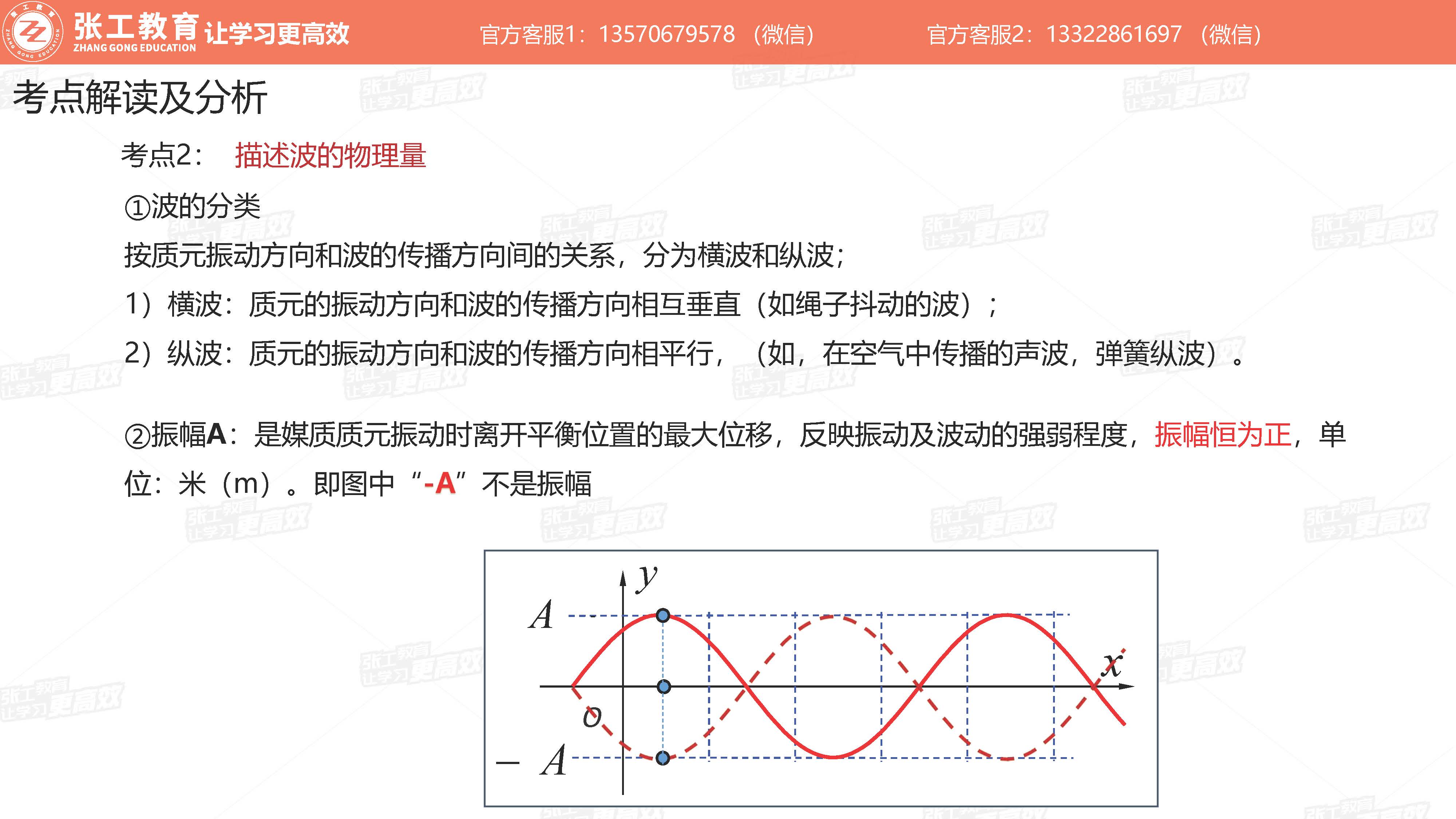
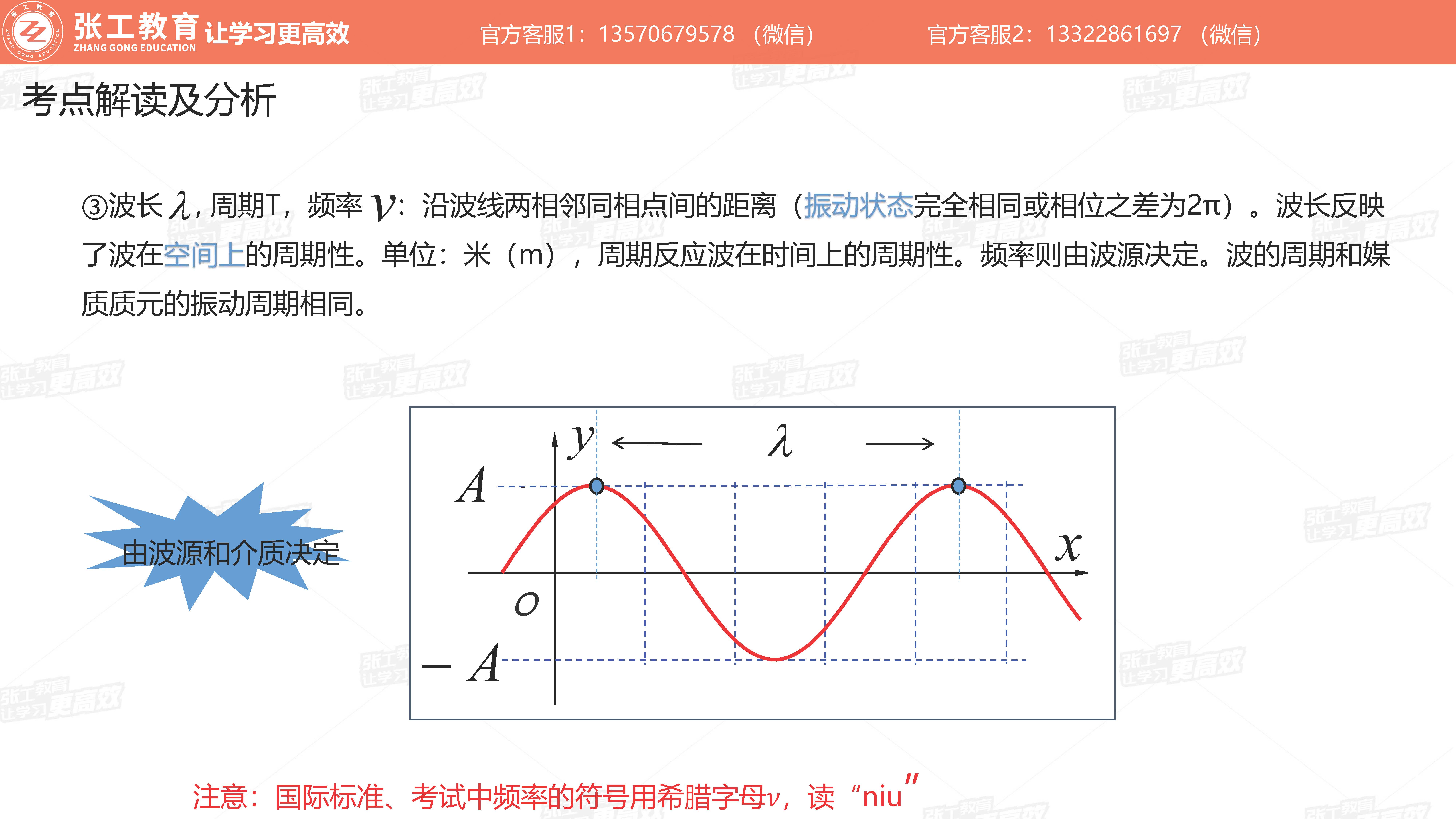
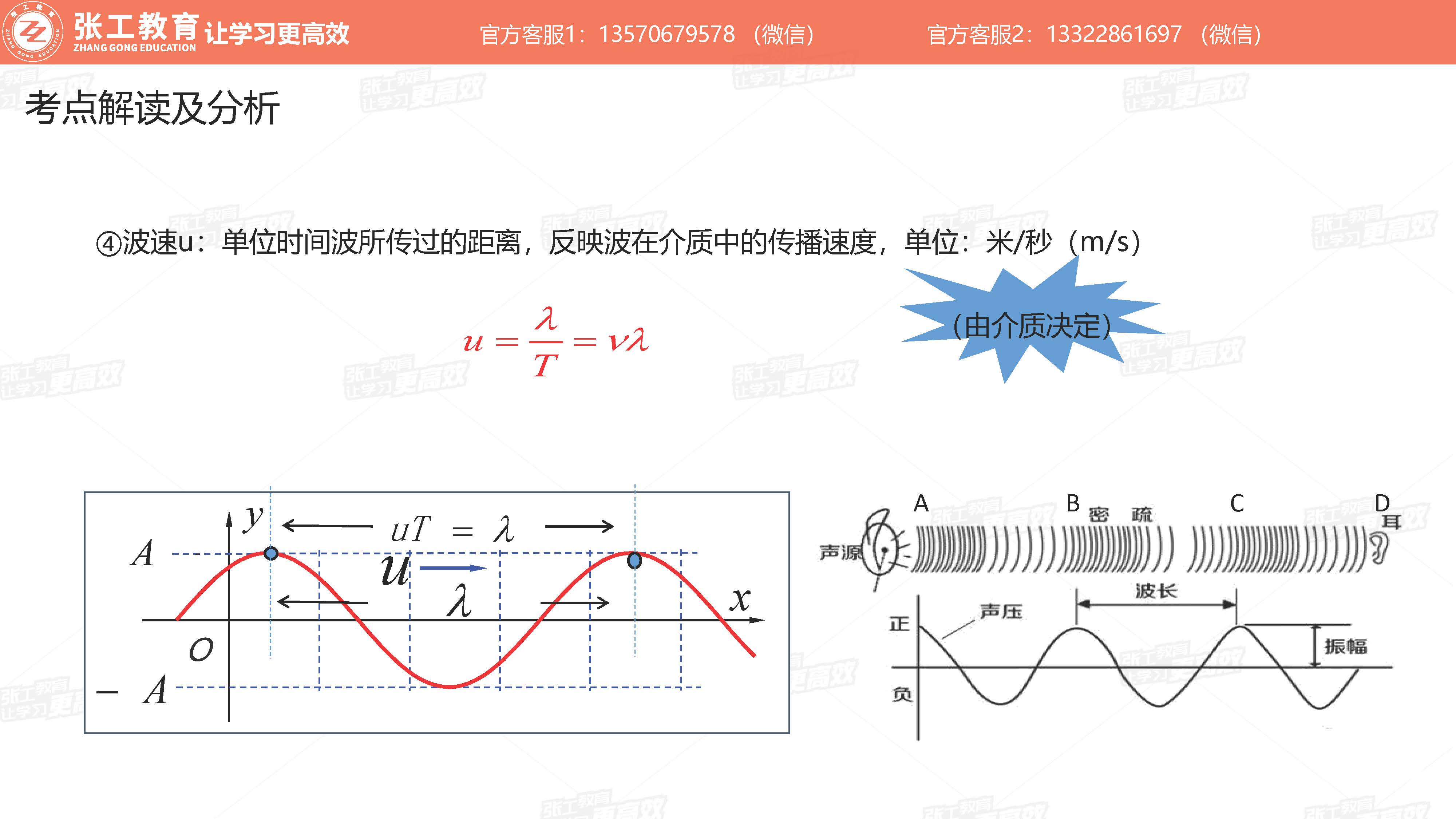
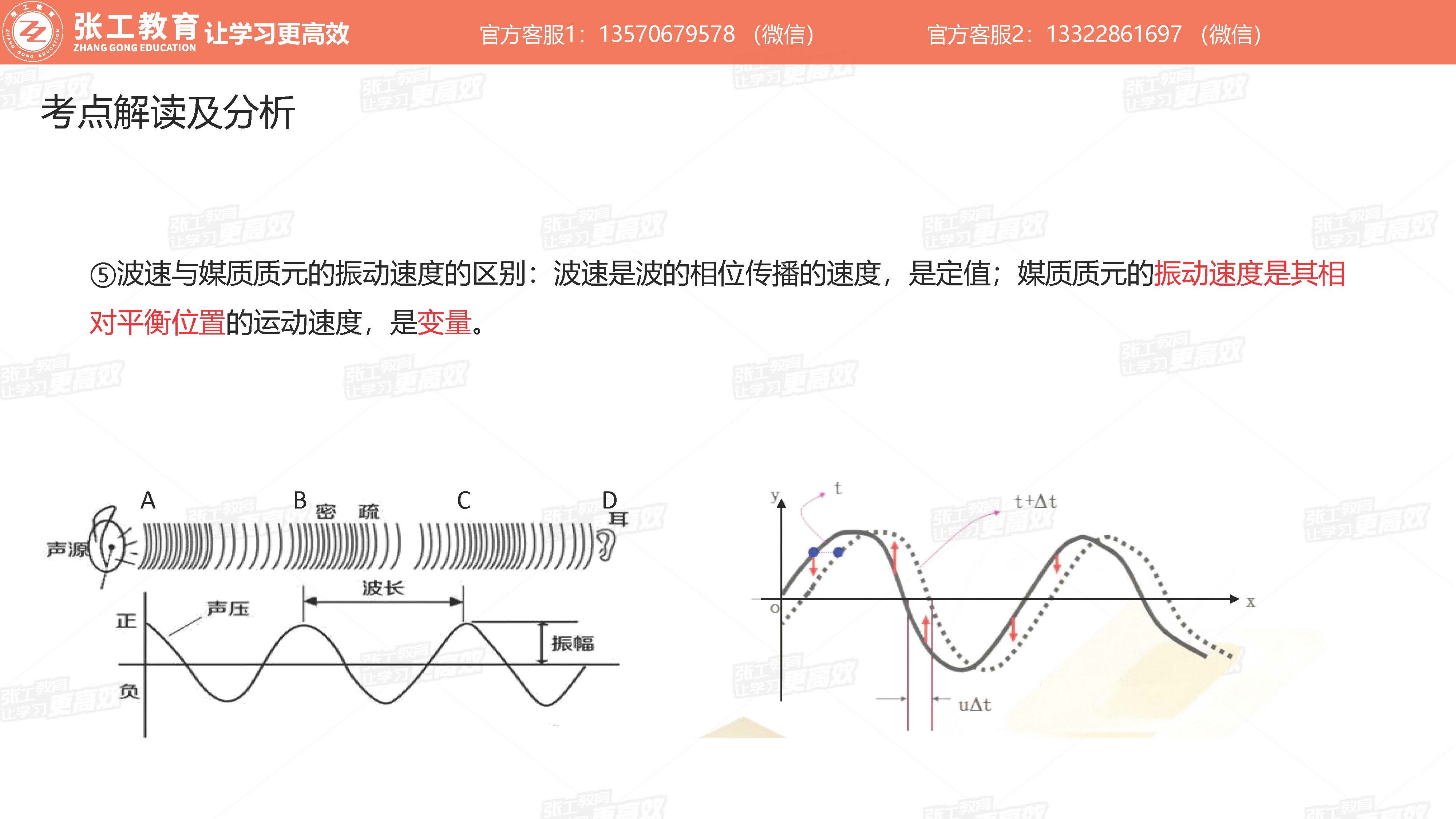
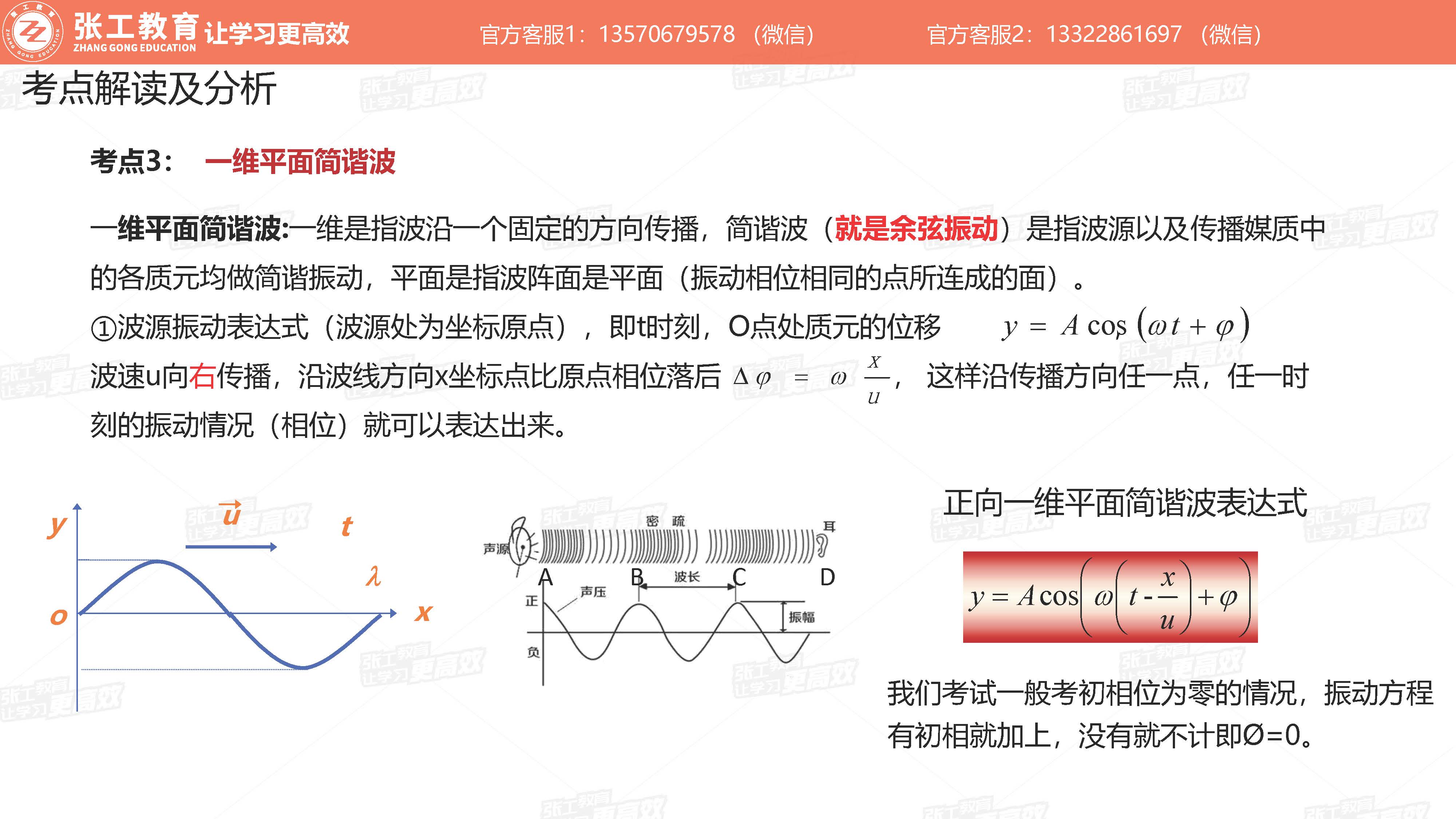
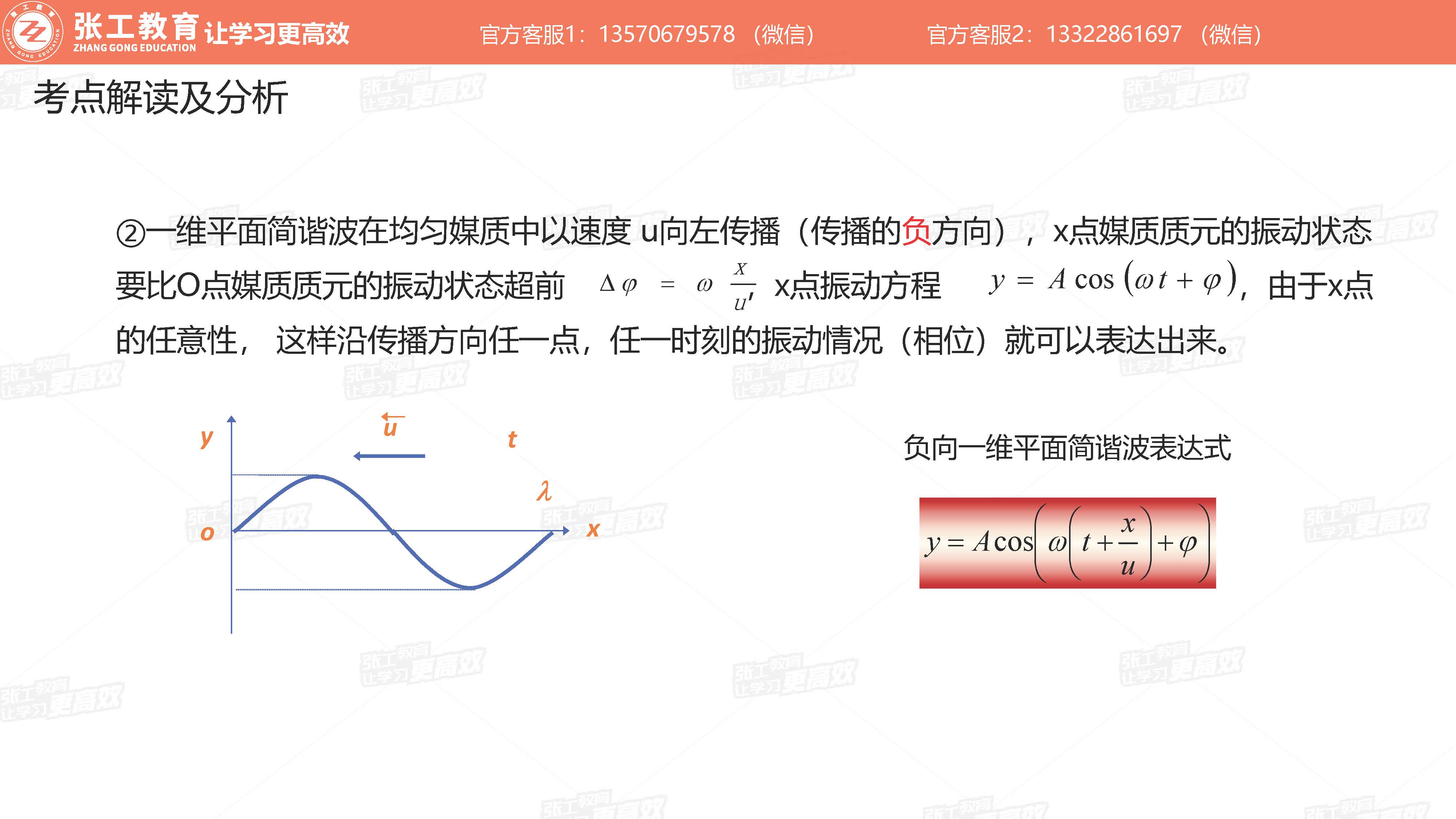
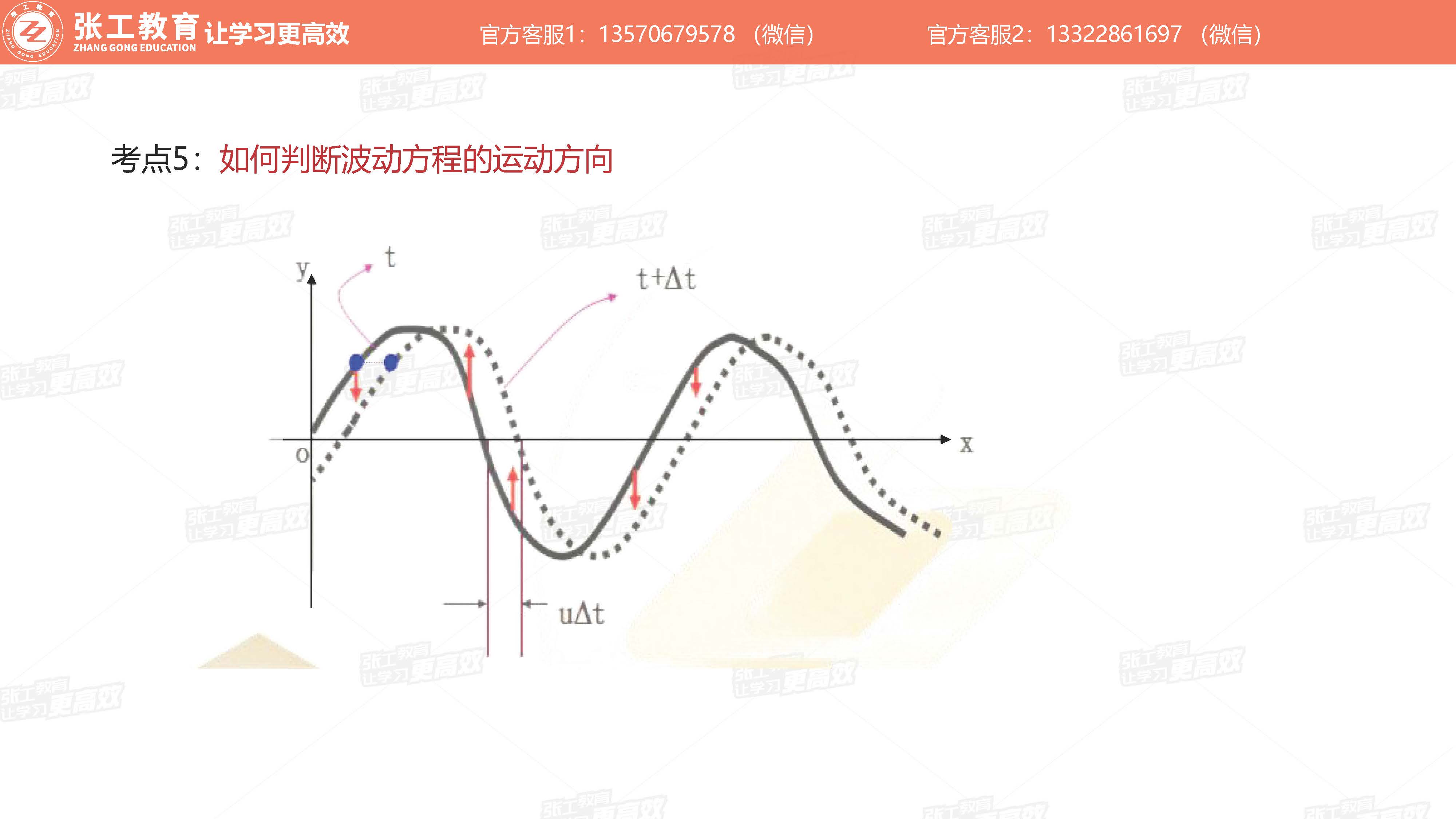
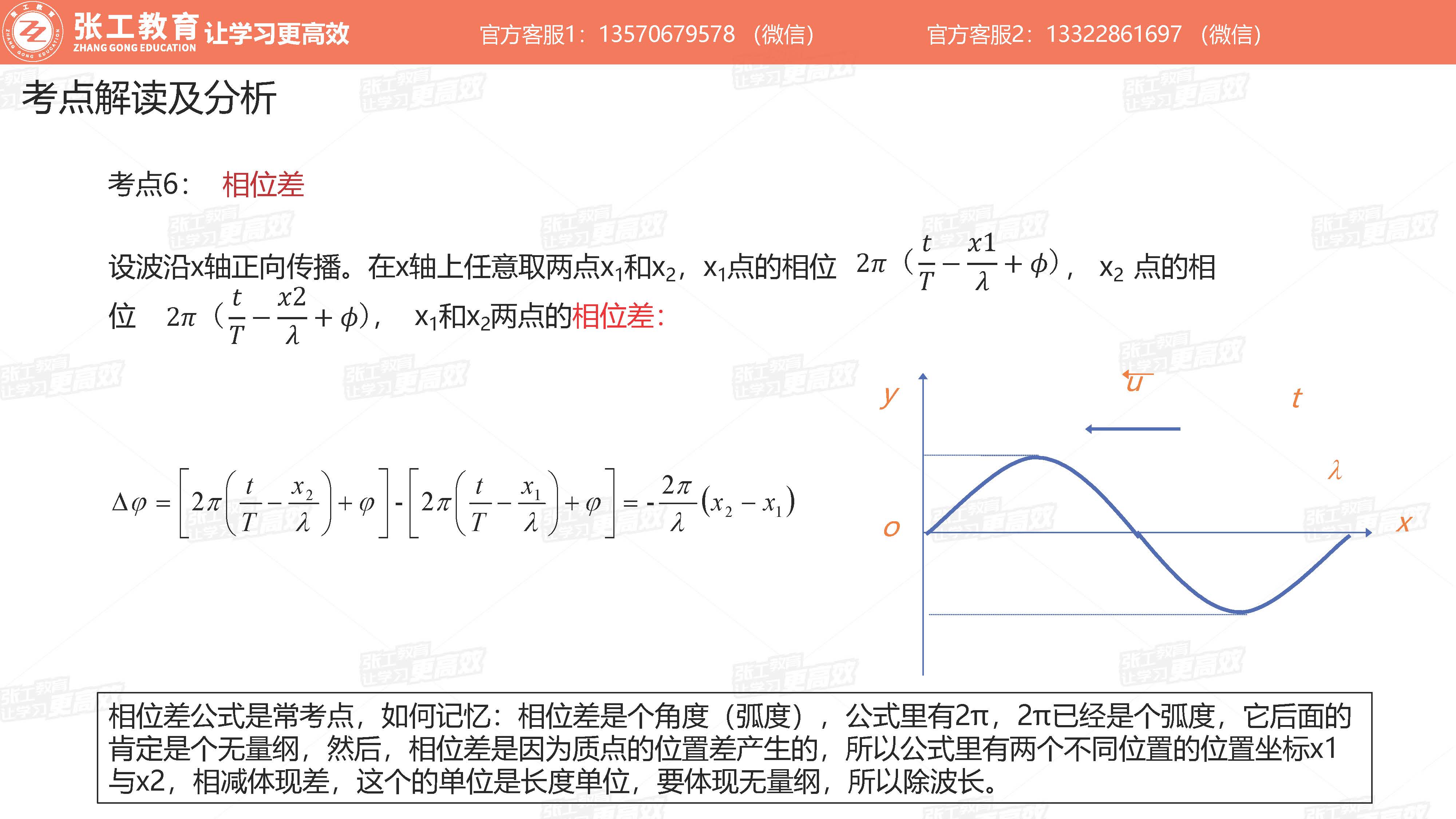
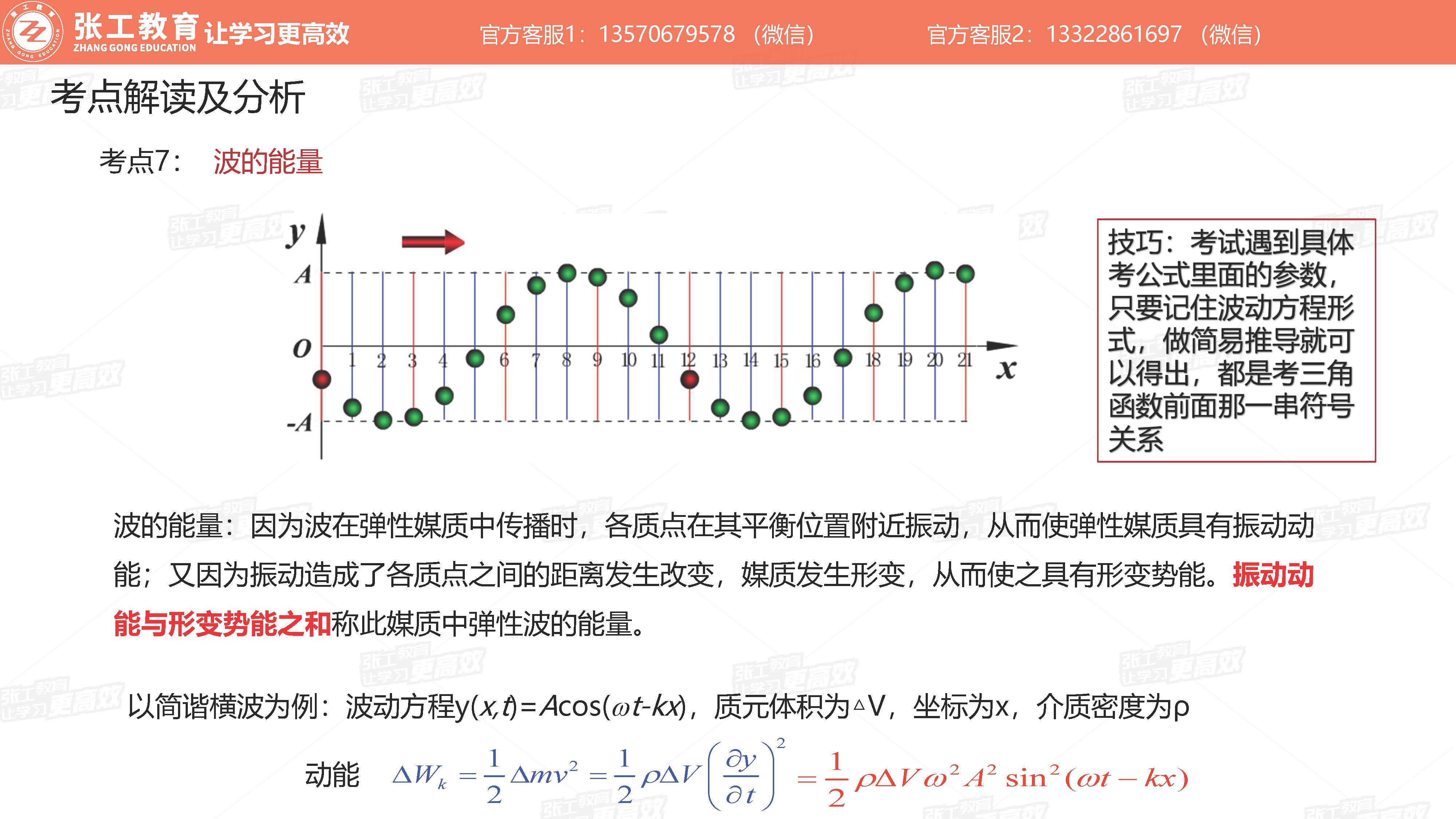
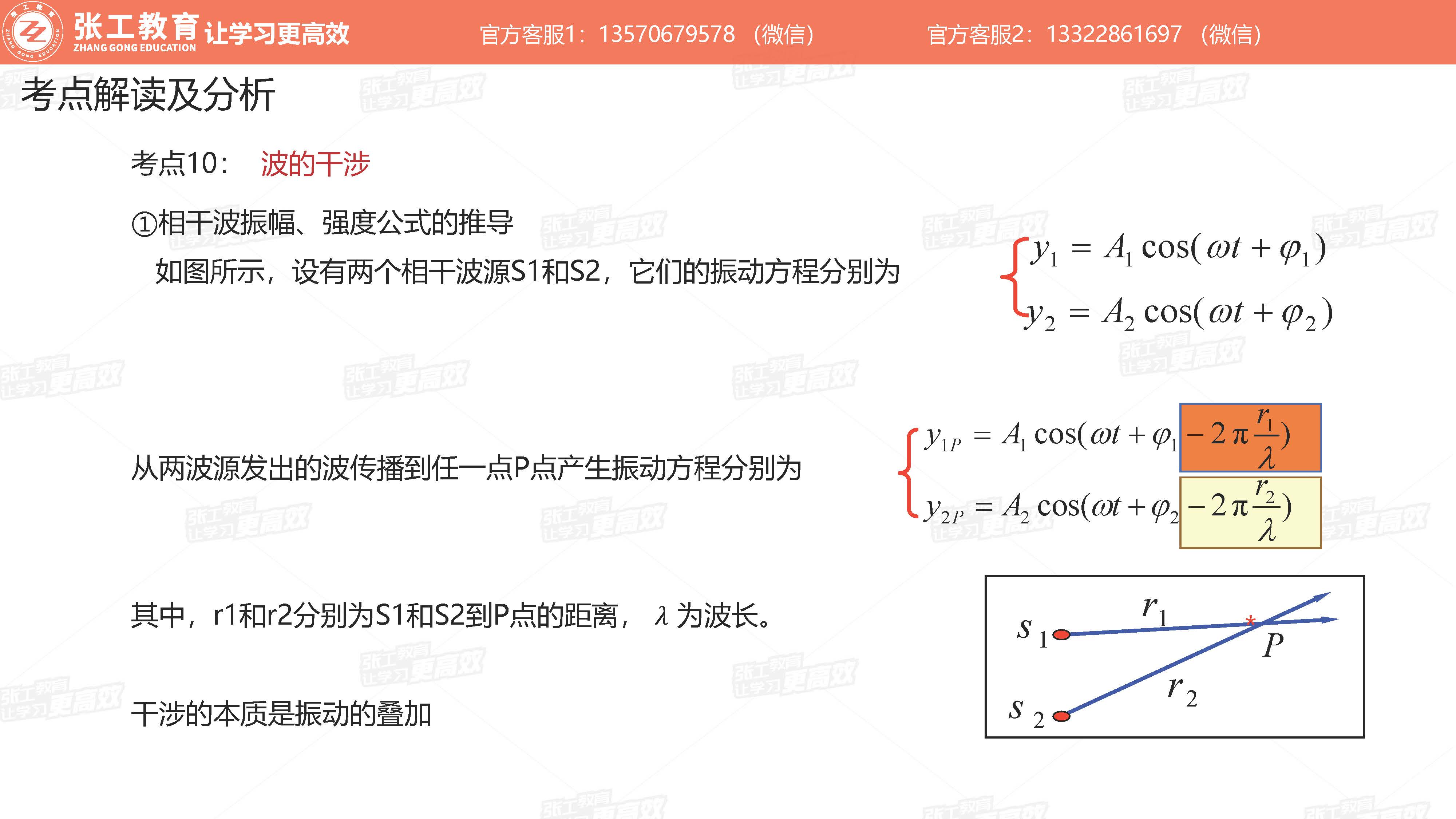
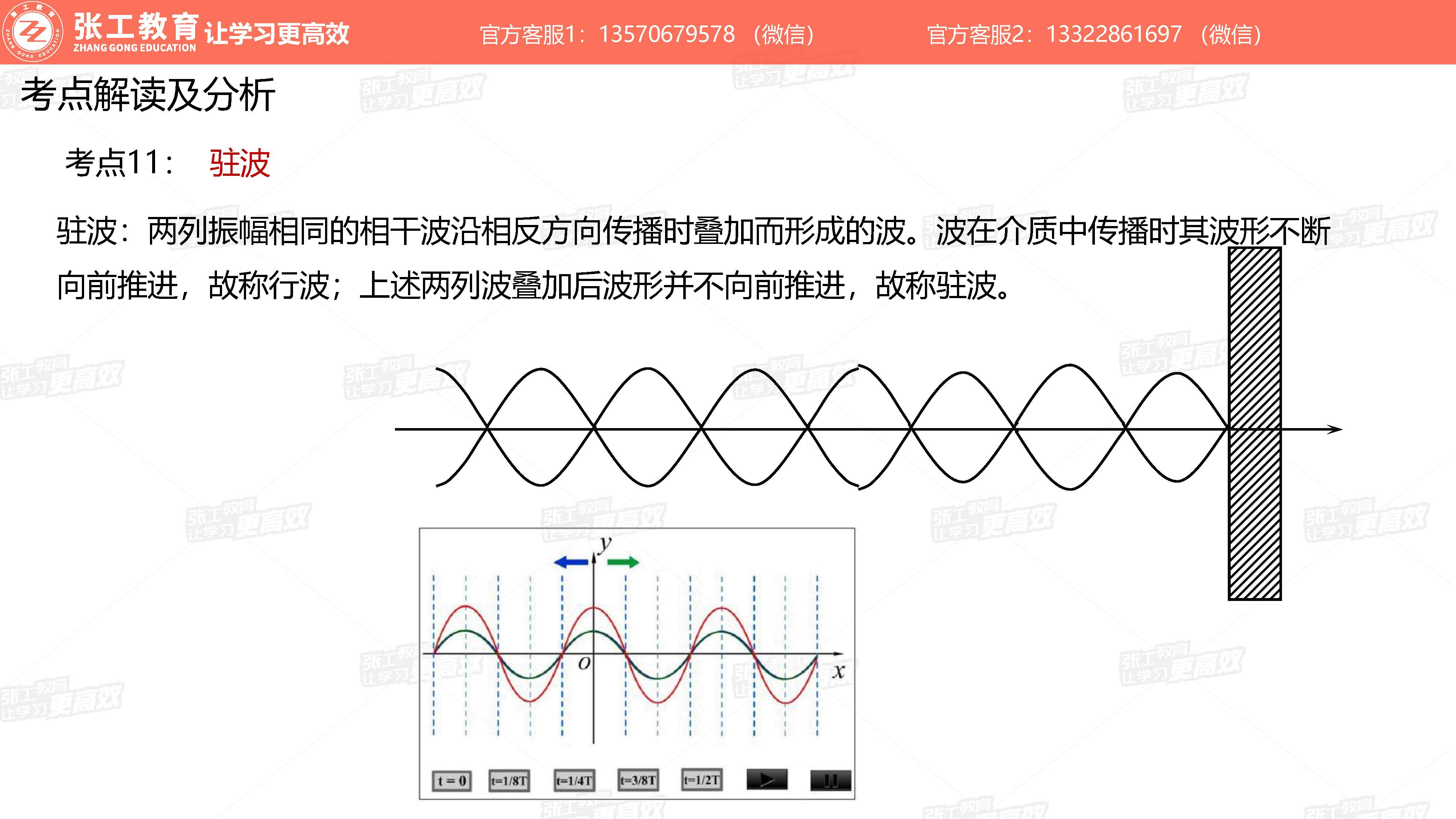
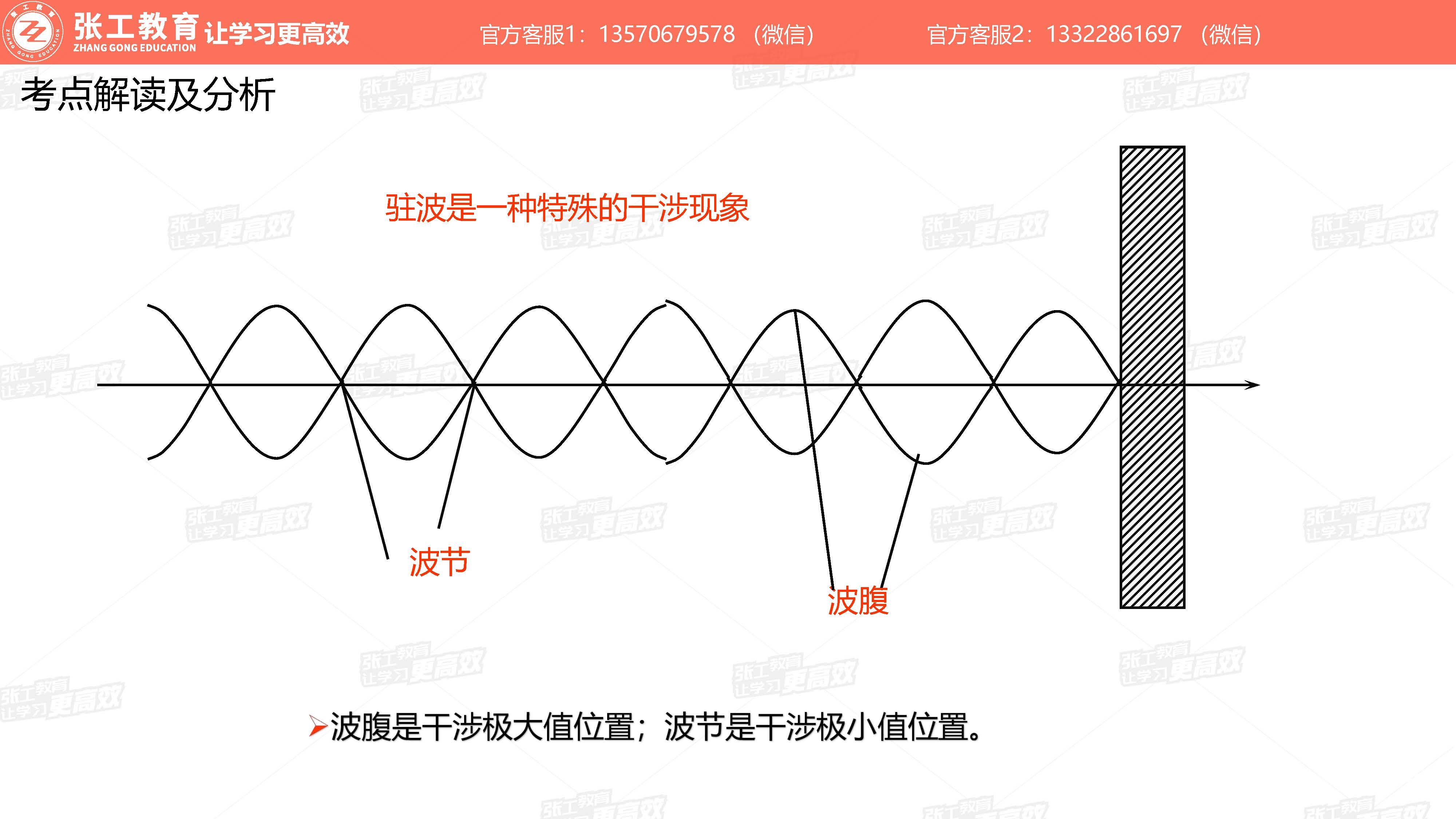
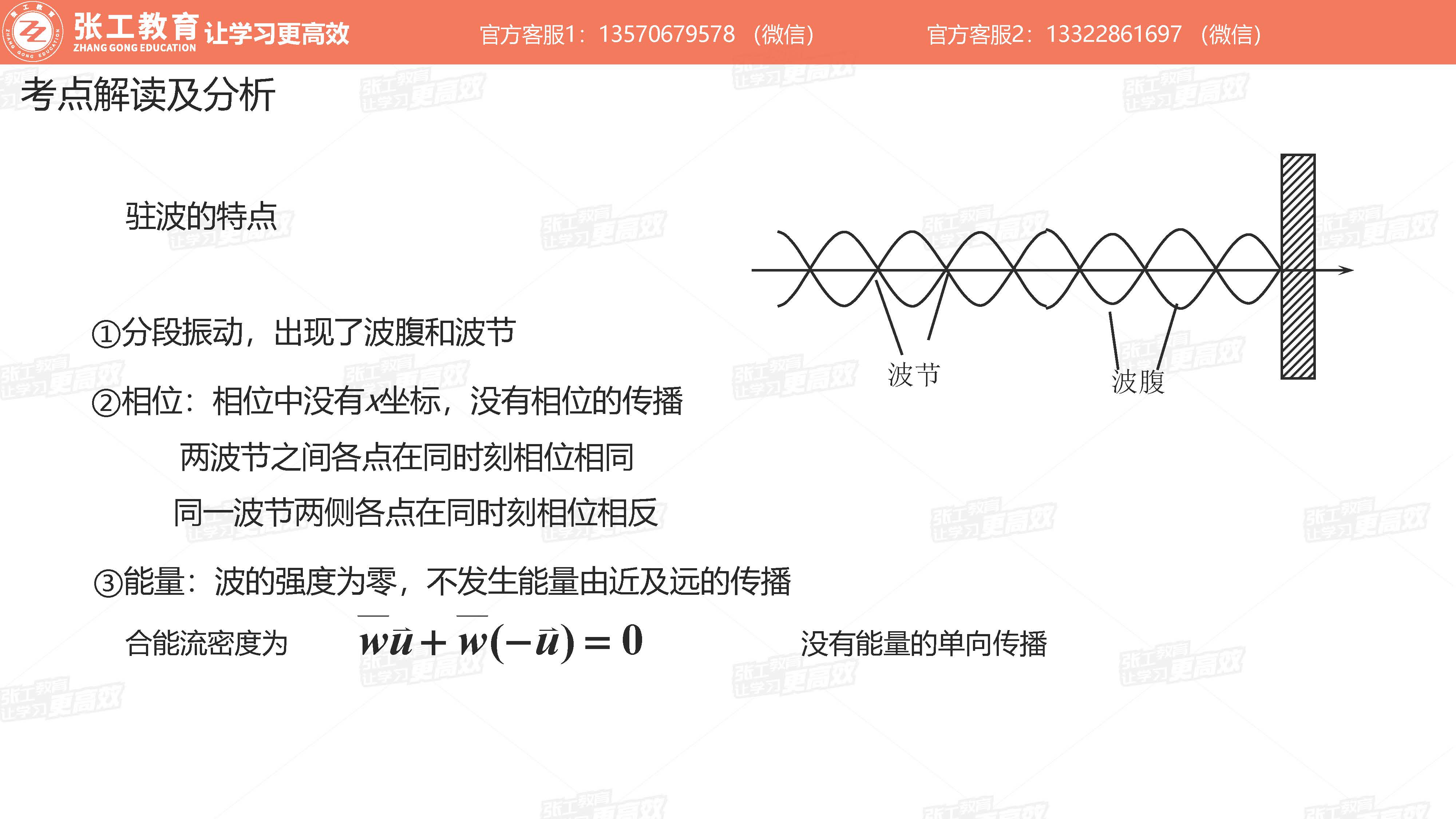
波动学(3-4分)